Kалькулятор жесткости воды ООО «Самарские коммунальные системы»
Жители г.о.Самара часто задают вопрос о величине жесткости воды при подборе посудомоечных и стиральных машин. Узнать значение жесткости водопроводной воды можно в разделе Качество, информация обновляется ежедневно. Кроме того вы можете ознакомиться с Картой жесткости воды г.о. Самара (Скачать)
В России жесткость измеряют в «градусах жесткости» (1 °Ж = 1 мг-экв/л = 1/2 моль/м3), а мировые производители используют принятые в своих странах единицы измерения. В связи с этим, для удобства жителей мы предлагаем воспользоваться калькулятором перевода значения жесткости воды из одной системы измерения в другую, чтобы правильно настроить свою бытовую технику.
Жесткостью воды называют совокупность химических и физических свойств воды, связанных с содержанием в ней растворенных солей кальция и магния («солей жесткости»). Общая жесткость складывается из временной и постоянной. Временную жесткость можно устранить кипячением воды, что обусловлено свойством некоторых солей выпадать в осадок, образуя так называемую накипь.
Основной фактор, влияющий на величину жесткости — растворение горных пород, содержащих кальций и магний (известняки, доломиты), при прохождении через них природной воды.
Поверхностные воды, в целом, имеют более низкие значения, чем подземные, и в течение года эти показатели не постоянны, увеличение может происходить из-за испарения воды, а уменьшение — в сезон дождей и в период таяния снега.
Единицы измерения жесткости воды в разных странах отличаются, поэтому ниже приведена таблица соответствия одной системы измерения другим. Например, 1°Ж (Россия) = 2,80°DH (Германия) или 1°DH (Германия) = 0,357°Ж (Россия).
| Ед. измерения | Россия | Германия | Великобритания | Франция | США | |
| Россия | °Ж | 1 | 2,80 | 3,51 | 5,00 | 50,04 |
| Германия | °DH | 0,357 | 1 | 1,25 | 1,78 | 17,84 |
| Великобритания | °Clark | 0,285 | 1 | 1. 43 43 |
14,3 | |
| Франция | °F | 0,20 | 0,56 | 0,7 | 1 | 10 |
| США | ppm | 0,02 | 0,056 | 0,070 | 0,1 | 1 |
Измерение жёсткости воды — эксклюзивный дистрибьютер Franke
Измерение жесткости воды
Люди в разных странах очень давно пришли к необходимости её нормировать, ибо высокая жесткость — это плохо: и трубы забиваются, и постирать толком невозможно. Но стали это делать в каждой стране по-своему, кто как, исходя из традиционных единиц измерения и способов определения ионов кальция и магния, ведь единых стандартизированных международных единиц тогда не было.
Известно, что нет ничего хуже вредных привычек — избавиться от них очень трудно! В кофейной литературе (хотя жесткость по сути своей понятие не из области кофе!) разных стран жесткость до сих пор измеряют в градусах, причем в каждой стране в своих собственных, отличных от всех остальных. Идентичны только русские и немецкие градусы жесткости, правда, давным-давно отменные в обеих этих странах, но упорно существующие в определении понятий.
В СССР до 1952 года использовали градусы жёсткости, совпадавшие с немецкими. В России для измерения жёсткости используется нормальная концентрация ионов кальция и магния, выраженная в миллиграммах эквивалента на литр (мг-экв/л). Один мг-экв/л соответствует содержанию в литре воды 20,04 миллиграмм Ca2+ или 12,16 миллиграмм Mg2+ (атомная масса делённая на валентность).
В других странах принято обозначать жесткость в УСЛОВНЫХ градусах:
Немецкие градусы (dGH)
1° = 1часть оксида кальция — СаО в 100000 частей воды, или 0.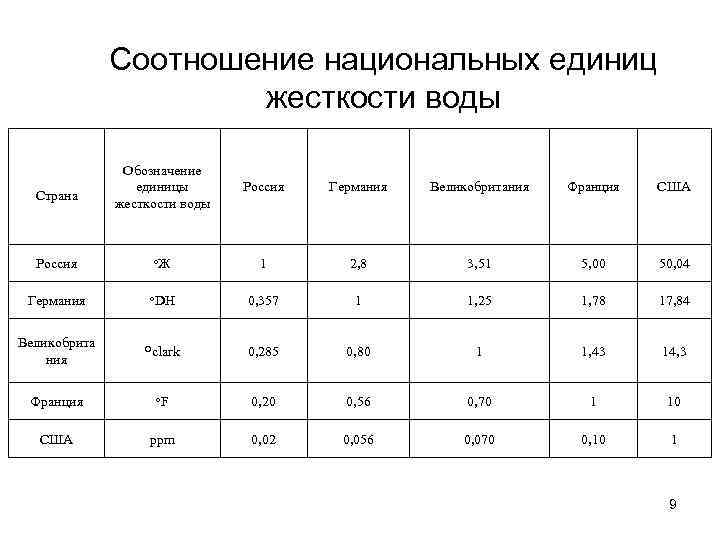 719 частей оксида магния — MgO в 100000 частей воды, или 10 мг СаО в 1 л воды, или 7.194 мг MgO в 1 л воды. dGH (dH) и dKH в настоящее время наиболее часто употребляется в аквариумистике как единица измерения жесткости, причем обозначение dGH — относится к общей жесткости, dKH — к карбонатной;
719 частей оксида магния — MgO в 100000 частей воды, или 10 мг СаО в 1 л воды, или 7.194 мг MgO в 1 л воды. dGH (dH) и dKH в настоящее время наиболее часто употребляется в аквариумистике как единица измерения жесткости, причем обозначение dGH — относится к общей жесткости, dKH — к карбонатной;
Французские градусы (fh)
1° = 1 часть CaCO3 в 100000 частей воды, или 10 мг CaCO3 в 1 л воды;
Американские градусы (usH)
1° = 1 гран (0.0648 г) CaCO3 в 1 галлоне (американском! 3.785 л) воды. Поделив граммы на литры получаем: 17.12 мг/л СаСО3. Однако есть еще одно определение американского градуса: 1 часть CaCO3 в 1000000 частей воды (в англоязычной литературе выражение концентрации, как 1 часть на 1 000 000 частей называют ppm — part per million (одна часть на миллион), и часто используют. На практике оно идентично 1мг/л). Таким образом этот 1 американский градус = 1мг CaCO3 в 1 л воды.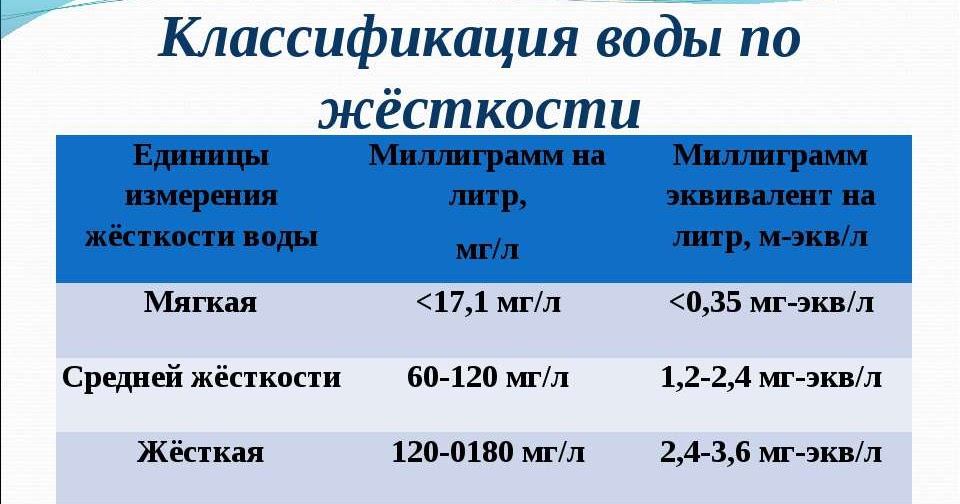
Английские градусы (Clark)
1° = 1 гран (0.0648 г) в 1 галлоне (английском! 4.546 л) воды = 14.254 мг/л CaCO3.
Чувствуете как все не просто?! Поэтому приведу таблицу, позволяющую сравнивать и переводить одни градусы жесткости в другие:
Таблица 1
| Наименование единиц | Градус жесткости | ||||
|---|---|---|---|---|---|
| немецкий | французский | американский | английский | ||
| 1 мг-экв/л | 1 | 2.804 | 5.005 | 50.045 |
3. 511 511 |
| 1 немецкий градус dH | 0.3566 | 1 | 1.785 | 17.847 | 1.253 |
| 1 французский градус | 0.1998 | 0.560 | 1 | 10,000 | 0.702 |
| 1 американский градус | 0.0200 | 0.056 | 0.100 | 1 | 0.070 |
| 1 английский градус | 0.2848 | 0.799 | 1.426 | 14.253 | 1 |
Каким способом и как можно измерять жесткость — Гидросистемы
Жесткость воды — мера содержания в воде растворенных солей кальция и магния. Источником их являются, в основном, известняки и доломиты. Различают постоянную жесткость, временную жесткость и общую жесткость воды.
Источником их являются, в основном, известняки и доломиты. Различают постоянную жесткость, временную жесткость и общую жесткость воды.
Постоянная жесткость воды (некарбонатная) Жп — обусловливается содержанием сульфатов, хлоридов и других (кроме бикарбонатов) солей кальция и магния. При нагревании или кипячении воды они остаются в растворе.
Временная жесткость воды (устранимая, карбонатная) Жвр — обусловливается содержанием бикарбонатов. При нагревании или кипячении воды бикарбонаты переходят в нерастворимые карбонаты, при этом жесткая вода умягчается. Обычно карбонатная жесткость составляет 70-80% от общей жесткости.
Общая жесткость воды Ж — определяется как суммарное содержание в воде солей кальция и магния, выражается как сумма карбонатной и некарбонатной жесткости: Ж = Жп + Жвр
Жесткая вода образует накипные отложения в водонагревательных и охлаждающих системах. В первом приближении это заметно на стенках, например, чайника. При хозяйственно-бытовом использовании жесткой воды наблюдается перерасход моющих средств вследствие образования осадка кальциевых и магниевых солей жирных кислот.
- Установки умягчения воды бытовые
- Установки умягчения воды промышленные
- Системы обратного осмоса бытовые
- Системы обратного осмоса промышленные
- Умягчители для стиральных машин
- Цены на установки умягчения, системы обратного осмоса, дозирующие станции (xls — 274 Kb)
- Спросить про установки умягчения, системы обратного осмоса, дозирующие станции (контактная информация)
Рекомендации по устранению жесткости воды
Высокая жесткость воды ухудшает ее органолептические свойства, жесткая вода неблагоприятно действует на организм человека. Также из-за высокой жесткости образуется накипь. Отсюда возникает необходимость устранения жесткости.
Одним из методов снижения жесткости воды является ионный обмен, который реализуется на автоматических установках умягчения воды серии RFS.
Устранение жесткости воды при помощи установок умягчения реализовано по принципу замещения ионов кальция и магния в воде ионами натрия. Происходит процесс умягчения воды — ионообменный процесс, приводящий к снижению ее жесткости.
Происходит процесс умягчения воды — ионообменный процесс, приводящий к снижению ее жесткости.
Удаление из воды солей жесткости происходит в фильтрующих колоннах. В процессе работы установки умягчения ионообменная емкость фильтрующего материала (катионита) уменьшается. Для восстановления обменной емкости катионита проводится регенерация. Регенерация осуществляется с использованием раствора соли (NaCl) и включает несколько стадий. Подробнее о работе установок снижения жесткости воды можно прочитать в разделе Каталог оборудования. Умягчение воды.
Существуют также установки умягчения воды непрерывного действия с использованием двух колонн, работающих поочередно. Они также подробно описаны на нашем сайте в рубрике Установки умягчения воды непрерывного действия.
Классификация природных вод по жесткости, бытовое определение жесткости воды
При оценке жесткости воды обычно воду характеризуют следующим образом:
| Вода | Жесткость, мг-экв/л |
| очень мягкая вода | до 1,5 мг-экв/л |
| мягкая вода | от 1,5 до 4 мг-экв/л |
| вода средней жесткости | от 4 до 8 мг-экв/л |
| жесткая вода | от 8 до 12 мг-экв/л |
| очень жесткая вода | более 12 мг-экв/л |
В соответствии с ГОСТ 4151-72 общая жесткость воды измерялась в мг-экв/л. С введением с 01.01.89 года изменения №1 единицей измерения жесткости являлся моль/м3.
С введением с 01.01.89 года изменения №1 единицей измерения жесткости являлся моль/м3.
С 01.01.2005 введен ГОСТ Р 52029-2003 Вода. Единица жесткости. По новому ГОСТу жесткость выражается в градусах жесткости (°Ж), что соответствует концентрации щелочноземельного элемента, численно равной 1/2 его моля, выраженной в мг/дм3 (г/м3). Ниже приводятся соотношения национальных единиц жесткости воды, принятых в других странах (ГОСТ Р 52029-2003).
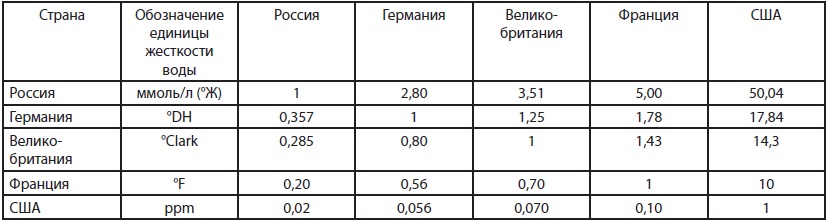
Соотношения национальных единиц жесткости воды
Данные взяты из текста ГОСТа
| Страна | Обозначение единицы жесткости | Россия | Германия | Великобритания | Франция | США |
| Россия | °Ж | 1 | 2,80 | 3,51 | 5,00 | 50,04 |
| Германия | °DH | 0,357 | 1 | 1,25 | 1,78 | 17,84 |
| Великобритания | °Clark | 0,285 | 0,80 | 1 | 1,43 | 14,3 |
| Франция | °F | 0,20 | 0,56 | 0,70 | 1 | 10 |
| США | ppm | 0,02 | 0,056 | 0,070 | 0,10 | 1 |
Примечания:
°Ж = 20,04 мг Ca2+ или 12,15 Mg2+ в 1 дм3 воды;
°DH = 10 мг CaO в 1 дм3 воды;
°F = 10 мг CaCO3 в 1 дм3 воды; ppm = 1 мг CaCO3 в 1 дм3 воды;
°Clark = 10 мг CaCO3 в 0,7 дм3 воды.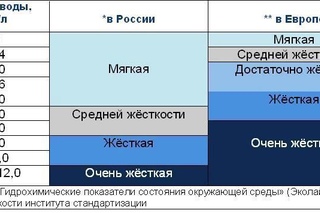
Численные значения жесткости измеренные в мг-экв/л, моль/м3, и °Ж, несмотря на различия в обозначении, равны между собой.
Источники:
Справочник по свойствам, методам анализа и очистке воды: В двух частях. Часть 1. / Киев: Наукова думка, 1980. — 680 с.
ГОСТ Р 52029-2003 Вода. Единица жесткости.
Жесткость воды — происхождение, виды, единицы измерения
Жесткость воды – это химическое свойство, которое определяет объем имеющихся в жидкости солей магния и кальция. Эта характеристика — одна из главных при определении качества воды. Как узнать жесткость воды? Она выявляется на основе проведенных анализов по определению степени пригодности воды для употребления человеком и использования в бытовых нуждах. Чем выше содержание солей, тем жидкость более жесткая.
Знание этой важной характеристики воды сохранит здоровье, красоту и продлит работу используемой техники.
Классификация воды по жесткости
Официальная международная единица измерения, используемая в системе СИ – моль на метр кубический. В нашей стране жесткость измеряют в градусах жесткости. Но часто эта характеристика выражается в объемной доле или массовым числом.
В нашей стране жесткость измеряют в градусах жесткости. Но часто эта характеристика выражается в объемной доле или массовым числом.
Чаще всего используется следующая единица: мг-экв./л или миллиэквивалент на литр.
Воду классифицируют на 4 типа:
— Меньше 2 мг-экв./л – мягкая;
— От 2 до 4 мг-экв./л – нормальная;
— От 4 до 6 мг-экв./л – жесткая;
— От 6 мг-экв./л – очень жесткая.
Эта классификация называемая американской.
Влияние жесткой воды на здоровье человека и домашних животных
Какой вред приносит жесткость воды? Чем выше показатель жесткости, тем мощнее вредное воздействие.
1. Жесткая вода содействует возникновению мочекаменной болезни. Соли из воды полностью не выводятся из органов человека.
2. Вода с высоким коэффициентом жесткости сушит кожный покров из-за возникновения «мыльных шлаков». Они не позволяют мылиться моющим средствам, не растворяясь в жесткой воде. Результат – закупоривание пор, вследствие чего возможен зуд, жжение, воспаление кожи.
Результат – закупоривание пор, вследствие чего возможен зуд, жжение, воспаление кожи.
3. На волосах разрушается жировая пленка, имеющая естественный характер. Волосы выглядят «не живыми», возникает зуд кожи головы, перхоть, возможно чрезмерное выпадение волос.
4. Время приготовления пищи увеличивается.
5. Аналогично жесткая вода действует и на домашних питомцев: появление мочекаменной болезни, проблемы с кожей, шерстью.
Влияние жесткой воды на бытовую технику
1. Наличие солей отрицательно сказывается на отмывании грязи разного происхождения. Расход средств увеличивается.
2. На посуде, сантехнике образуются разводы, твердый налет, плохо отмываемый и способствующий разрушению поверхности предметов.
3. В электроприборах в процессе нагревания соли кристаллизируются (накипь), что способствует ускоренному выходу приборов из строя.
4. Возможно появление пятен, разводов на выстиранных вещах, потускнение цвета, рисунков.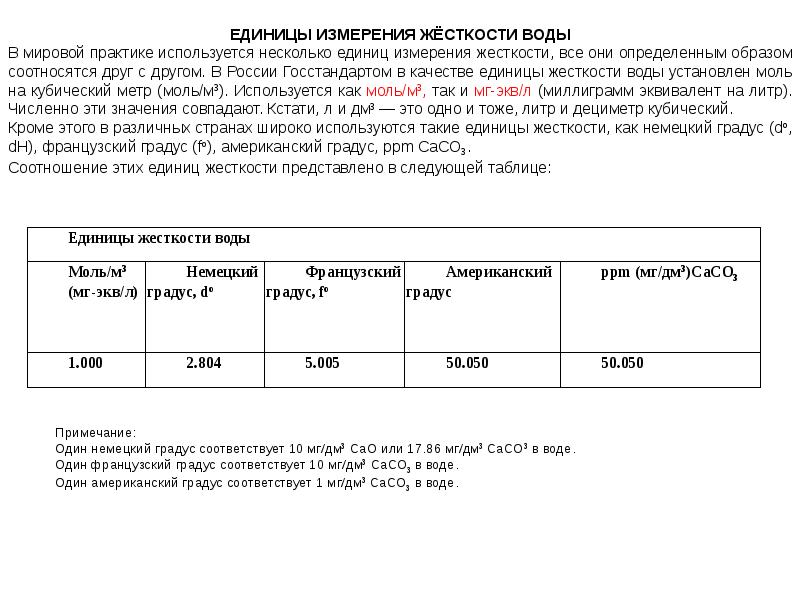 Ткань становится неэластичной, грубой.
Ткань становится неэластичной, грубой.
5. Водопроводные трубы, трубы тепло коммуникаций, крупные приборы общего пользования также страдают от жесткой воды.
Определение жесткости воды
Самый точный метод определения общей жесткости воды – сдать анализы в лабораторию, например в СанЭпидемСтанцию.
Как узнать жесткость воды в домашних условиях? Можно приобрести в магазинах, где продаются кофе-машины или в зоомагазинах специальные тест-полоски. Они опускаются в воду. Цвет реагента, нанесённого на полоску, меняется.
Простой, но не точный метод состоит в следующем. При мытье рук мыло пенится быстро – вода мягкая. Если пенообразование не явное, то вода может быть жесткой.
Для устранения жесткости воды в домашних условиях можно использовать различные фильтры.
Для питья и приготовления пищи самый удобный способ – приобретение бутилированной воды, такой как «Королевская вода», отвечающая всем необходимым для потребления характеристикам..gif)
Единицы измерения жесткости — Справочник химика 21
ТАБЛИЦА ПЕРЕСЧЕТА ЕДИНИЦ ИЗМЕРЕНИЯ ЖЕСТКОСТИ [c.18]Пересчет единиц измерения жесткости воды [c.16]
Единицы измерения жесткости. Единой международной единицы измерения жесткости не существует. Различные страны условно принимают свои единицы. Очень часто жесткость воды измеряют градусами жесткости. [c.189]
Единицы измерения жесткости воды мг-экв/л Градусы жесткости [c.33]
Единицы измерения жесткости. Единой международной единицы измерения жесткости не существует. Различные страны условно принимают свои единицы. [c.187]
Градус жесткости (°Ж)—единица измерения жесткости воды, соответствующая содержанию 0,01 г СаО в 1 л воды. [c.259]
Вода, Методы химического анализа. Единица измерения жесткости Полевой метод физико-химического анализа питьевой воды [c. 17]
17]
В табл. 149 дан пересчет различных единиц измерения жесткости в миллиграмм-эквиваленты. [c.446]
Единица измерения жесткости мг-эпв/л Нем. град. Франц. град. Англ. град. Амер. град. [c.218]
Единицы измерения жесткости Миллиграмм- эквивалент Немецкий градус Французский градус Английский градус [c.76]
Что такое жесткость воды и чем она обусловлена Какие виды жесткости различают Что служит единицей измерения жесткости Какими методами определяют жесткость и в чем сущность этих методов Какие ионы и почему мешают определению жесткости [c.191]
Различают временную, постоянную и общую жесткость воды . Общая жесткость воды равна сумме постоянной и временной жесткости. За единицу измерения жесткости мг-экв1л) в настоящее время принимают содержание одного миллиграмм-эквивалента (мг-экв) кальция (Са) или магния (Mg) в 1 л воды. [c.130]
За единицу измерения жесткости до 1952 г.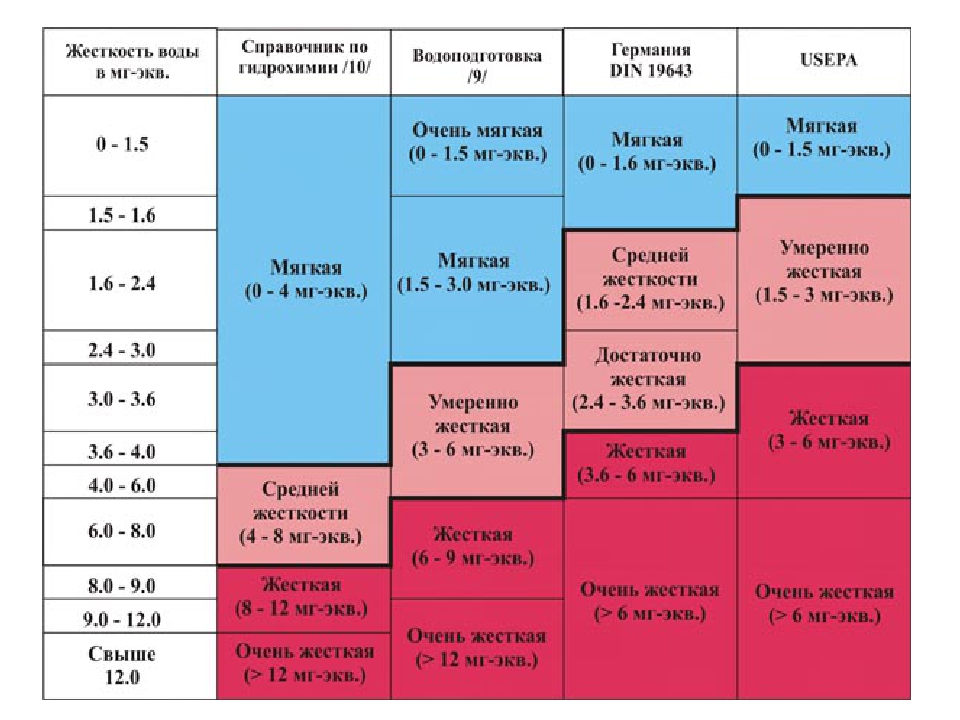 в СССР принимали [c.431]
в СССР принимали [c.431]Пример. Определено в 1 л воды окиси кальция (СаО) 90 мг, окиси магния (MgO) в пересчете на окись кальция — 25 мг. Общая жесткость 90-f— -25=115 жг=11,5 , в пересчете на новую единицу измерения жесткости [c.278]
Единицы измерения жесткости при изгибе пересчитаны из фунт/дюйм в кН/мм .) На кривой, имеющей форму, которую и следовало ожидать из теоретического анализа, наблюдается уменьшение кажущегося модуля упругости значительно ниже действительного модуля упругости с уменьшением отношения lid, особен- [c.206]
Приведите электронные формулы атома магния и кальциа 2.. Как изменяются основные свойства гидроксидов элементов главной подгруппы второй группы периодичес]сой системы Чем это можно объяснить фЗ. Почему гидроксид магния растворяется в соляной кислоте и в растворе хлорида аммонил ф4. Почему карбонаты кальция и магния растворяются в прирсдной воде Составьте уравнения соответствующих реакций. фЗ. Чем обусловливается общая, «временная и постоянная жесткость воды фи. Что принимается за единицу измерения жесткости воды в СССР ф7. На титрование 100 мл воды в присутствии метилового оранжевого затрачено 3,4 мл 0,0988 н. раствора серной кислоты. Вычислите жесткость воды в мэкв/л. ф8. Жесткость воды равна 2,9 мэкв/л. Какое, количество соды нужно прибавить к 1 м такой в( ды для устранения жесткости ф9. Составьте уравнение реакции, происходящей при отвердении гашеной извести. ф10. Как получают негашеную известь В чем заключается процесс гашения навести Выразите происходящие реакции уравнениями. ф11. Почему нельзя осадить полностью гидроксид магния действием гидроксида аммония ф12. Составите уравнения следующих реакций [c.171]
фЗ. Чем обусловливается общая, «временная и постоянная жесткость воды фи. Что принимается за единицу измерения жесткости воды в СССР ф7. На титрование 100 мл воды в присутствии метилового оранжевого затрачено 3,4 мл 0,0988 н. раствора серной кислоты. Вычислите жесткость воды в мэкв/л. ф8. Жесткость воды равна 2,9 мэкв/л. Какое, количество соды нужно прибавить к 1 м такой в( ды для устранения жесткости ф9. Составьте уравнение реакции, происходящей при отвердении гашеной извести. ф10. Как получают негашеную известь В чем заключается процесс гашения навести Выразите происходящие реакции уравнениями. ф11. Почему нельзя осадить полностью гидроксид магния действием гидроксида аммония ф12. Составите уравнения следующих реакций [c.171]
ГОСТ 6055—51. Вода. Методы химического анализа. Единица измерения жесткости. [c.320]
Прежде жесткость воды выражали условными единицами, называемыми градусы жесткости . Приводимая в тексте единица измерения жесткости воды введена ГОСТ 6055—51. [c.355]
[c.355]
Количественно жесткость воды в ряде стран выражают в градусах. В СССР за единицу измерения жесткости воды принимают миллиграмм-эквивалент Са + или Mg на 1 л воды, что отвечает содержанию 20,04 мг/л Са или 12,16 мг/л Mg +. По степени жесткости подразделяют воду на мягкую — менее [c.259]
Количественно жесткость воды в ряде стран выражают в градусах. В СССР за единицу измерения жесткости воды принимают миллиграмм-эквивалент Са + или на 1 л воды, что отвечает содержанию 20,04 мг л Си или 12,16 мг л Mg +. [c.209]
Единицы измерения жесткости [c.446]
Раньше применяли также и другие единицы измерения жесткости воды. Так называемые немецкие градусы показывают содержание в граммах СаО в 10Э л воды при этом все соли как Са», так и Mg условно пересчитываются на СаО. [c.319]
Смещение элемента системы иногда оценивают угловым перемещением в радианах. В соответствии с этим меняют и единицу измерения жесткости.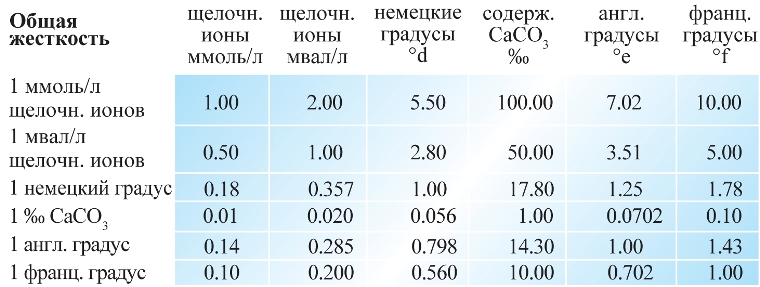 [c.27]
[c.27]
Что принимается за единицу измерения жесткости воды в СССР Что такое немецкий и французский градусы жесткости воды 10. На титрование 100 мл воды в присутствии метилоранжа затрачено 3,4 мл 0,0988 н. раствора серной кислоты. Вычислить жесткость воды в мг-9кв1л, немецких и французских градусах. 11. Жесткость воды равна 2,9 мг-жв1л. Какое количество соды нужно прибавить к 1 м этой воды для устранения жесткости. 12. Написать уравнение реакции, происходящей при отвердении гашеной извести. 13. При помощи каких химических реакций можно осуществить следующие процессы [c.224]
ГОСТ 5605-50. Предприятия промышленные. Метод определения содержания паров сероуглерода в воздухе, 3642 ГОСТ 5606-50. Предприятия промышленные. Метод определения содержания аммиака в воздухе, 3643 ГОСТ 5609-50. Предприятия промышленные. Метод определения содержания нетоксичной пыли в воздухе, 3644 ГОСТ 5610-50. Предприятия промышленные. Метод определения содержания сероводорода в воздухе, 3645 ГОСТ 5612-50.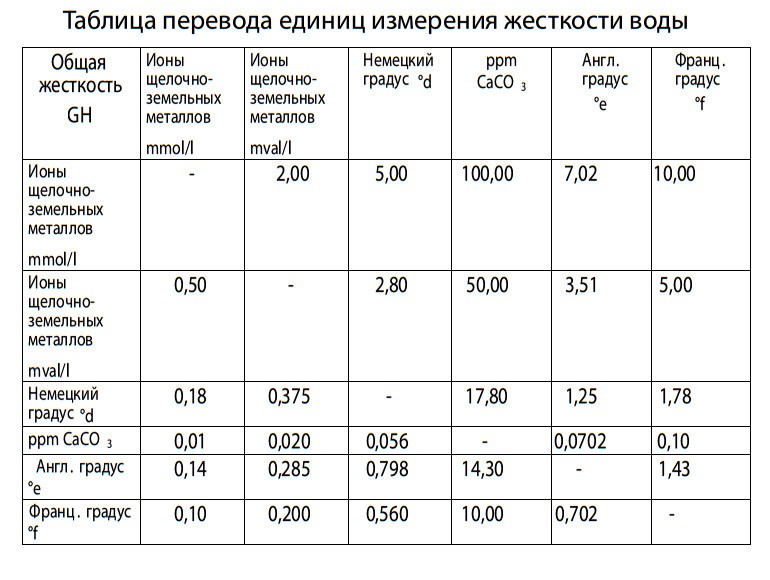 Предприятия промышленные. Метод определения содержания окиси углерода в воздухе, 3646 ГОСТ 5637-51. Олово, Методы химичес] )го анализа. Взамен ГОСТ 860-41 в части методов химического анализа. о647 ГОСТ 6012-51. Никель, Метод спектрального анализа, 3648 ГОСТ 6055-51. Вода, Методы химического анализа, Единица измерения жесткости, 3649 Гохштейн Я. П. О восстановлении кислородосодержащих анионов [Сг04 , комплексных ионов молибдена] на капельном ртутном катоде, Тр, Комис, по аналит. химии (АН СССР, Отд,-ние хим, наук), 1949, 2, с. 54— 64. 3650 Гранберг И. А., Сухенко К. А., Развязкина К. А. [и др.]. Спектральный анализ магнитных сплавов. Зав. лаб,, 1951, 17, № 9, с, 1093—1096, 3651 Грановский И. В. и Дружинин Ф. Г. Фторид ный метод определения окиси кальция в мартеновских и доменных шлаках. Зав.лаб., [c.148]
Предприятия промышленные. Метод определения содержания окиси углерода в воздухе, 3646 ГОСТ 5637-51. Олово, Методы химичес] )го анализа. Взамен ГОСТ 860-41 в части методов химического анализа. о647 ГОСТ 6012-51. Никель, Метод спектрального анализа, 3648 ГОСТ 6055-51. Вода, Методы химического анализа, Единица измерения жесткости, 3649 Гохштейн Я. П. О восстановлении кислородосодержащих анионов [Сг04 , комплексных ионов молибдена] на капельном ртутном катоде, Тр, Комис, по аналит. химии (АН СССР, Отд,-ние хим, наук), 1949, 2, с. 54— 64. 3650 Гранберг И. А., Сухенко К. А., Развязкина К. А. [и др.]. Спектральный анализ магнитных сплавов. Зав. лаб,, 1951, 17, № 9, с, 1093—1096, 3651 Грановский И. В. и Дружинин Ф. Г. Фторид ный метод определения окиси кальция в мартеновских и доменных шлаках. Зав.лаб., [c.148]
Шапкин И. Ф. Новая единица измерения жесткости и щелочности [воды]. Энергет. бюл. (М-во нефт. пром-сти). 1952, № 8, с. 27. 6227 [c.237]
Французские градусы Г= 1 г СаСОз в 100 л воды. Английские градусы 1°= 1 г СаСОз в 70 л воды. Американские градусы Г=1 г СаСОз в 1000 л воды. В СССР до 1951 г. пользовались для измерения жесткости немецким градусом жесткости, но в 1951 г. установлена новая единица измерения жесткости, выраженная в миллиграмм-эквивалентах на литр воды. По ГОСТ 6055—51 1 мг-экв жесткости соответствует содержанию 20,04 мг л Са + или 12,16 мг/л Mg +. [c.190]
Английские градусы 1°= 1 г СаСОз в 70 л воды. Американские градусы Г=1 г СаСОз в 1000 л воды. В СССР до 1951 г. пользовались для измерения жесткости немецким градусом жесткости, но в 1951 г. установлена новая единица измерения жесткости, выраженная в миллиграмм-эквивалентах на литр воды. По ГОСТ 6055—51 1 мг-экв жесткости соответствует содержанию 20,04 мг л Са + или 12,16 мг/л Mg +. [c.190]
Градус жесткости воды — единица измерения жесткости — определяет содержание в воде солей окиси. кальция (СаО). За один градус принято содержание одной части СаО в 100 000 частей воды или 1 мг в литре. ГОСТом установлен в 1951 г. новый стандарт, выраженный так миллиграммэквивалент на литр или микрограммэквивалент на литр (1 мг-экв1л) равен 2,804 немецких градуса. [c.63]
Раньше за единицу измерения жесткости воды принимался градус жесткости (1°), соответствующий содержанию в 1 д воды 10 мг окиси калыщя (извести) СаО или 7,14 мг окиси магния MgO, или эквивалентного количества других солей кальция и магния. [c.130]
[c.130]
Количественно жесткость воды в ряде сУтран выражают в градусах. В СССР за единицу измерения жесткости воды принимают миллиграмм-эквивалент Са + или g + на 1 л воды, что отвечает содержанию 20,04 мг/л Са + или 12,16 мг/л M.g +. По степени жесткости подразделяют воду на мягкую — менее 4 мг-экв/л, средней жесткости — 4—8 мг-экв/л и очень жесткую 8—12 мг-экв/л и выше. [c.209]
Жесткость воды — важный показатель качества воды
Жесткость водыявляется важным показателем качества воды. Vodalab рассказывает о жесткости воды, ее видах и способах умягчения воды.
ЖЕСТКОСТЬ ВОДЫ
Жесткая вода чаще всего ассоциируется с накипью на дне чайника или ощущением мыла на руках после мытья рук, некоторые испытывают ощущение «жестких волос». По этому критерию люди обычно оценивают качество воды. В этой статье мы рассмотрим жесткость со стороны физики и химии, изучим ее свойства, разновидности, влияние на здоровье человека и способы ее устранения жесткости воды.
Вода, содержащая большое количество солей кальция
Эффект жесткой воды
Жесткость воды — это концентрация растворённых в ней солей магния (Mg) и кальция (Ca): гидрокарбонатов, хлоридов и сульфатов. Проще говоря, жесткой называется вода, содержащая в себе большое количество солей. Почему воду назвали «жесткой»? Женщины в старину стирали вещи на берегу рек и озер, в воде которых содержат кальций, отчего ткань становилась жесткой на ощупь.
Жесткость воды делится на 3 вида:
- Карбонатная, т.е. временная. Она ликвидируется с помощью обычного кипячения воды и обусловлена гидрокарбонатами кальция и магния Са(НСО3)2; Mg(НСО3)2.
- Некарбонатная, т.е. постоянная. Возникает из-за присутствия других солей, например CaSO4, Ca(Cl)2, MgSO4, Mg(Cl)2. При кипячении воды не устраняется.
- Общая. Представляет собой суммарную концентрацию ионов кальция и магния. Представляет собой сумму карбонатной и некарбонатной жесткости.
Единицы измерения жесткости:
Не существует единой единицы измерения жесткости. В России, в соответствии с Госстандартом, в качестве единицы жесткости воды установлен моль на кубический метр (моль/м3). В Германии — 2.8DH°; во Франции — 5F°; в Америке — 50.05 ppm CaCO3.
В России, в соответствии с Госстандартом, в качестве единицы жесткости воды установлен моль на кубический метр (моль/м3). В Германии — 2.8DH°; во Франции — 5F°; в Америке — 50.05 ppm CaCO3.
Классификация воды по жесткости:
| Характеристика | Жесткость, мг-экв/л |
| очень мягкая вода | до 1,5 мг-экв/л |
| мягкая вода | от 1,5 до 4 мг-экв/л |
| вода средней жесткости | от 4 до 8 мг-экв/л |
| жесткая вода | от 8 до 12 мг-экв/л |
| очень жесткая вода | более 12 мг-экв/л |
Согласно требованиям СанПиН 2.1.4.1074-01 жесткость питьевой воды должна быть не выше 7 мг-экв/л.
Влияние на здоровье человека:
Как же влияет жесткая вода на наш организм? Медики связывают появление мочекаменной болезни именно с этой особенностью воды. Но на данный момент официального подтверждения этой гипотезе нет. Но мы знаем, что слишком жесткая вода неблагоприятно влияет на органолептические свойства воды, придавая ей горьковатый вкус. Также жесткая вода сушит нашу кожу и волосы. Однако, полностью переходить на мягкую воду не рекомендуется. Наш организм нуждается в солях кальция и магния для укрепления сердечно-сосудистой системы. А вот комнатные растения лучше поливать мягкой или талой водой.
Но мы знаем, что слишком жесткая вода неблагоприятно влияет на органолептические свойства воды, придавая ей горьковатый вкус. Также жесткая вода сушит нашу кожу и волосы. Однако, полностью переходить на мягкую воду не рекомендуется. Наш организм нуждается в солях кальция и магния для укрепления сердечно-сосудистой системы. А вот комнатные растения лучше поливать мягкой или талой водой.
Способы борьбы с жесткой водой:
Для смягчения жесткости воды специалисты рекомендуют приобрести умягчители, которые являются самыми эффективными в борьбе с солями жидкости. Также существует несколько способов смягчения воды в домашних условиях, самым простым и привычным из которых является кипячение воды.
Для борьбы с постоянной жёсткостью воды используют такой метод, как вымораживание льда. Необходимо просто постепенно замораживать воду. Когда примерно 90% жидкости превратится в лед, нужно разморозить его обратно, а соли останутся в оставшейся незамороженной жидкости.
При выборе степени жесткости воды лучше придерживаться середины. Самым оптимальным является использование воды средней жесткости для приготовления пищи и мягкой воды для гигиенических процедур. А чтобы ваша бытовая техника не страдала от повышенной жесткости, лучше приобрести умягчитель.
Самым оптимальным является использование воды средней жесткости для приготовления пищи и мягкой воды для гигиенических процедур. А чтобы ваша бытовая техника не страдала от повышенной жесткости, лучше приобрести умягчитель.
Заказать анализ воды на жесткость вы можете на нашем сайтеvodalab. Каждый из представленных на сайте анализов содержит исследование воды на жесткость.
О других загрязнителях воды, таких как железо, мутность и марганец, вы также можете узнать подробнее в нашем блоге.
что это и как влияет на вкус кофе
Чашка фильтр-кофе на 98,5% состоит из воды, а её качество имеет большое значение для кофе.
Общая и карбонатная жесткость — ключевые параметры, которые определяют качество воды. За общую жесткость отвечают хлорид кальция (CaCl2), сульфат кальция (CaSO4), хлорид магния (MgCl2) и сульфат магния (MgSO4). За карбонатную — бикарбонат калия (KHCO3) и бикарбонат натрия (NaHCO3).
За карбонатную — бикарбонат калия (KHCO3) и бикарбонат натрия (NaHCO3).
Соли магния и кальция помогают извлечь из кофе больше вкуса и не выпадают в осадок при кипячении воды. А вот с бикарбонатами все не так просто. Вода, которая перенасыщена карбонатами, образует накипь. При кипячении воды соли выпадают в осадок и могут привести к поломке кофемашины.
Казалось бы, выбирайте воду с низким содержанием карбонатов, и проблема решена. Но недостаточное количество карбоната кальция в воде может вызвать коррозию бойлера и трубок. А главное — содержание бикарбонатов влияет на воспринимаемую кислотность кофе.
Мы уже рассказывали о том, как состав воды влияет на экстракцию. Теперь разбираемся, как карбонатная жесткость влияет на pH воды и вкус кофе.
Как карбонатная жесткость влияет на pH водыЧтобы стабилизировать pH воды, нужна буферная система. А основная буферная система в воде — это как раз бикарбонаты Ca(HCO3)2. Если в воде будет много бикарбонатов, они «уничтожат» положительную кислотность кофе.
Если в воде будет много бикарбонатов, они «уничтожат» положительную кислотность кофе.
В кофе насчитывается более 40 органических кислот. От вида и соотношения кислот зависит вкус напитка: будет ли это приятная искристая кислотность или неприятная уксусная. Для этого в индустрии спешелти проводят эксперименты с ферментацией — процессом, при котором количество кислот в кофе увеличивается.
От вида и соотношения кислот в кофе зависит вкус напитка. А состав воды определяет экстракцию этих кислот
Большинство кислот в кофе слабые. Это значит, что даже незначительные отклонения в составе воды могут сильно повлиять на вкусовые свойства. Если взять воду с разным исходным ppm — уровнем минерализации — ppm кофе на выходе будет одинаковым, а вот вкус разным. Все потому, что разная вода по-разному растворяет вещества из кофе.
Итак, вкус кофе меняется в зависимости от параметров воды. Когда уровень pH понижается, растет кислотность воды, и кофе получается кислым. Если уровень pH повышается, во вкусе кофе появляется горечь. Чтобы уровень pH оставался стабильным, в воде должны содержаться бикарбонаты. Нужно только подобрать оптимальное соотношение минеральных веществ в воде.
Если уровень pH повышается, во вкусе кофе появляется горечь. Чтобы уровень pH оставался стабильным, в воде должны содержаться бикарбонаты. Нужно только подобрать оптимальное соотношение минеральных веществ в воде.
Specialty Coffee Association выпустила стандарты, согласно которым допустимый диапазон карбонатной жесткости: ± 40 ppm. Карбонатная жесткость измеряется по шкале KH, а общая — по шкале GH.
Целевые показатели воды от SCA
Спецификация расплывчата, непонятно, что означает «плюс-минус» в отношении диапазона KH. Максвелл Колонна-Дэшвуд и Кристофер Хэндон в книге «Вода для кофе. Наука. История. Руководство» провели серию экспериментов, чтобы проверить, что будет со вкусом кофе при разных соотношениях общей и карбонатной жесткости воды.
Максимальная общая жесткость и минимальная карбонатная жесткость (точка А)Проблема. Недостаточно буфера, чтобы экстрагировать сильные кислоты.
Недостаточно буфера, чтобы экстрагировать сильные кислоты.
Кислотность в кофе получается очень приглушенной.
Максимальная карбонатная жесткость и минимальная общая жесткость (точка B)Проблема. Не экстрагируются сложные вкусоароматические вещества. Не сформировалось тело напитка. Буфер нейтрализовал слабые положительные кислоты.
Вкус плоский, едкий, пережаренный.
Минимальная общая жесткость и минимальная карбонатная жесткость (точка С)Проблема. Вода становится слишком пустой. Она не может извлечь нужное количество соединений из кофе из-за недостаточного количества минералов. Плохо сформированное тело кофе.
Вкус пустой, слегка уксусный.
Максимальная карбонатная жесткость и максимальная общая жесткость (точка D)Проблема. Из-за максимальной KH вероятность образования накипи резко возрастает. Чтобы компенсировать такую высокую буферную способность, требуется очень высокая экстракция, поэтому GH тоже должна быть высокой. Из-за высокого содержания минеральных веществ вода быстро переэкстрагирует кофе.
Чтобы компенсировать такую высокую буферную способность, требуется очень высокая экстракция, поэтому GH тоже должна быть высокой. Из-за высокого содержания минеральных веществ вода быстро переэкстрагирует кофе.
Вкус горький, терпкий, пустой.
Итак, чтобы получить сбалансированный вкус, в кофе должны быть кальций, магний и небольшое содержание буфера.
Исследуя карту воды, Максвелл Колонна-Дэшвуд и Кристофер Хэндон постарались найти границы для каждого параметра. Эти точки не являются конкретными значениями, но находятся в пределах погрешности около 10 ppm
Как показали эксперименты Максвелла Колонна-Дэшвуда и Кристофера Хэндона, для стабильного вкуса кофе в воде должно быть сохранено небольшое количество буфера. В качестве отправной точки вы можете использовать соотношение GH и KH 2:1.
Если баланс нарушен, проверьте состав воды и параметры водоподготовки. Для домашнего приготовления кофе выбирайте бутилированную воду с карбонатной жесткостью 50-70 мг/л при рН 7,0. Бариста могут менять параметры водоподготовки для кофемашины в сторону уменьшения или увеличения солей в воде.
Бариста могут менять параметры водоподготовки для кофемашины в сторону уменьшения или увеличения солей в воде.
Мы уже рассказывали о том, как выбрать воду для кофе, как контролировать качество воды, которая попадает в кофемашину и как измерить вкус кофе по специальным параметрам. Чтобы понять, как состав вашей воды влияет на готовый напиток, ориентируйтесь на вкус кофе. Экспериментируйте, пробуйте разную воду и меняйте параметры водоподготовки с учетом желаемого вкуса. Так вы сможете получить кофе с яркой приятной кислотности.
Что запомнить-
В воде должно содержаться небольшое количество бикарбонатов — до 70 ppm. Они помогают держать pH воды под контролем, что положительно влияет на приятную кислотность кофе.
-
Правильно подбирайте воду для заваривания кофе. Обращайте внимание на показатель «гидрокарбонат» на этикетке, оптимальное значение — 50-70 мг/л при рН 7,0.

-
Важно не оценивать общую и карбонатную жесткость по отдельности. Их соотношение влияет на вкус кофе. Рекомендуемое соотношение GH и KH 2:1.
-
При высоком содержании карбоната киcлотность будет не цитрусово-ягодной, а плоской и землистой. При низком содержании карбоната вкус получается уксусным и кислым.
Жесткость воды
Существуют разные типы жесткости воды:
| ● TH | – | Общая жесткость | |
| ● CH | – | Карбонатная жесткость | (временная жесткость) |
| ● NCH | – | Негарбонатная жесткость | (постоянная твердость) |
| ● PsH | – | Псевдотвердость |
Общая жесткость TH
Общая жесткость определяется как молярные концентрации всех мульти- -валентных катионов в воде (т. е.е. все, кроме одновалентных катионов):
е.е. все, кроме одновалентных катионов):
| (1) | Общая жесткость TH = Σ многовалентных катионов |
На практике он часто используется как сумма двух наиболее важных пресноводных катионов, кальция и магния:
| (1а) | TH ≈ [Ca] + [Mg] |
Но это только приблизительное значение, хотя и хорошее. Правильная формула (согласно определению в 1 ):
| (1б) | TH = [Ca] + [Mg] + [Sr] + [Ba] + [Fe] + [Mn] + [Al] +… |
Используется несколько шкал жесткости воды.Например, он может быть выражен в мэкв / л (единицы СИ), или в ppm CaCO 3 , или в немецких градусах жесткости:
.| (2а) | TH, мг-экв / л | = | 2 × ([Ca в мМ] + [Mg в мМ]) |
| (2б) | TH в миллионных долях | = | 100,1 × ([Ca в мМ] + [Mg в мМ]) |
| (2c) | TH дюйм ° d | = | 0.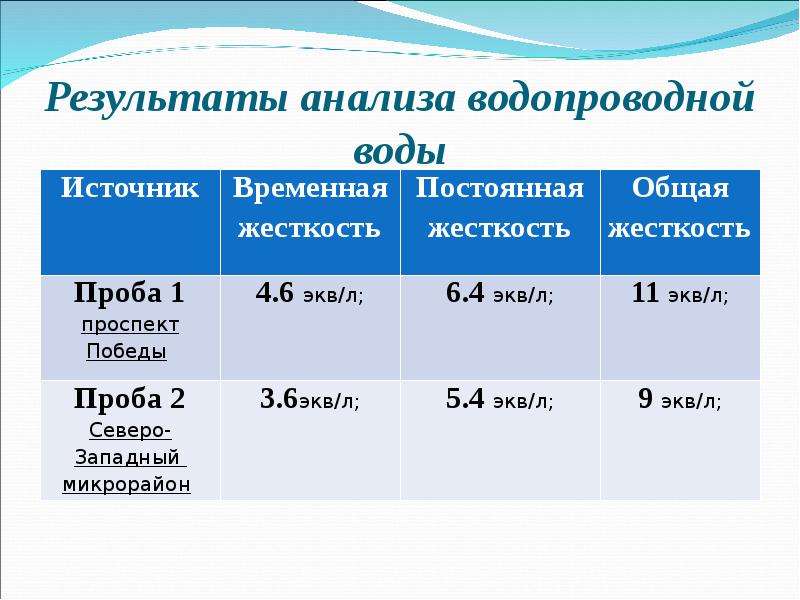 1339 × [Ca в мг / л] + 0,2307 × [Mg в мг / л] 1339 × [Ca в мг / л] + 0,2307 × [Mg в мг / л] |
Правила разговора с другими устройствами приведены в таблице ниже. Общая жесткость TH используется для классификации водных растворов по четырем категориям жесткости воды.
Примечание. Если концентрации ионов Ca и Mg выражены как «ppm CaCO 3 », 1a также отображается в форме:
| (3) | Общая жесткость TH = жесткость по кальцию + жесткость по магнию |
Карбонатная жесткость CH
В то время как общая жесткость в 1 определяется содержанием катионов , существует также противоположная точка зрения, взятая из содержания анионов , которые делят общую жесткость на карбонатную жесткость CH (временную жесткость) и некарбонатную жесткость. NCH (постоянная твердость):
| (4) | Общая жесткость TH = CH + NCH |
Карбонатная жесткость напрямую зависит от щелочности:
| (5а) | CH в мэкв / л | = | [Алк в мэкв / л] |
| (5б) | CH, ° dH | = | 2. 809 × [Алк в мэкв / л] 809 × [Алк в мэкв / л] |
Это означает, что в химии воды термины карбонатная жесткость и щелочность (т. Е. Щелочность M или общая щелочность) являются синонимами:
| (6) | Карбонатная жесткость CH = Щелочность |
Программа вычисляет TH и CH и отображает обе величины в таблицах результатов, как показано здесь.
Нкарбонатная жесткость NCH
И общая жесткость, и щелочность (т.е. карбонатная жесткость) — общие параметры анализа воды. Некарбонатная жесткость — согласно 4 — разница обоих величин:
| (7) | NCH = TH — CH |
Карбонатная жесткость называется временной жесткостью , потому что карбонаты Ca и Mg осаждаются в виде минералов при нагревании, тогда как Ca и Mg, связанные с сульфатами, хлоридами или нитратами, не осаждаются при нагревании (поэтому NCH называется постоянной твердостью ) .
Альтернативное толкование. Некарбонатная жесткость — это мера превышения сильных кислот над сильными основаниями:
| (8) | NCH = сильные кислоты — сильные основания |
При анализе воды сильных кислот проявляют себя в присутствии некарбонатных анионов, таких как сульфат, хлорид, нитрат. С другой стороны, сильных оснований обозначены одновалентными катионами (например,грамм. Na, K, аммоний). Таким образом, 8 преобразуется в
| (9) | NCH [мэкв / л] ≈ (2 × сульфат + хлорид + нитрат) — (Na + K + аммоний) |
, где измеренные концентрации следует вводить в ммоль / л.
Псевдотвердость PsH
Три величины, TH, CH и NCH, образуют стандартную терминологию жесткости воды почти во всех учебниках. Однако проблема возникает, если измеренная щелочность (т.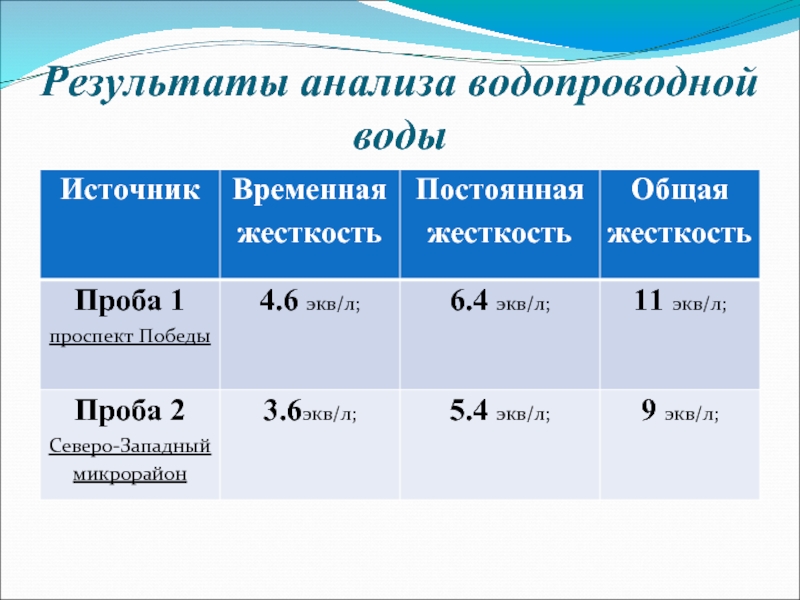 е.е. CH) превышает общую жесткость: CH> TH. В этом частном случае 4 становится бессмысленным.
е.е. CH) превышает общую жесткость: CH> TH. В этом частном случае 4 становится бессмысленным.
Чтобы решить эту проблему, терминология твердости должна быть расширена за счет дополнительной величины — псевдотвердости PsH (или «кажущейся твердости»). Он определяется как «отрицательный NCH» и выражается обратной цифрой 8 :
.| (10) | PsH = сильные основания — сильные кислоты = — NCH |
| (11) | PsH [мэкв / л] ≈ (Na + K + аммоний) — (2 × сульфат + хлорид + нитрат) |
Другими словами, PsH — это часть карбонатной жесткости, которая принадлежит одновалентным катионам (Na, K, аммоний).
Расширение общего отношения твердости
За счет дополнительного количества PsH мы можем расширить «стандартное уравнение твердости» (4):
| (12) | Жесткость воды: TH + PsH = CH + NCH |
Важно отметить, что PsH и NCH исключают друг друга в приведенной выше формуле: либо сильные основания перевешивают сильные кислоты (тогда NCH = 0), либо наоборот (тогда PsH = 0).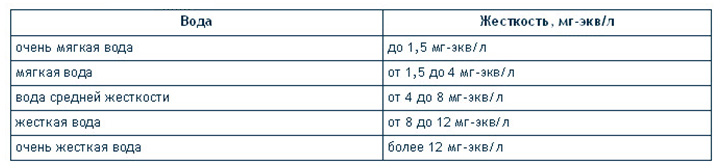 Таким образом, 12 становится:
Таким образом, 12 становится:
| (13а) | TH ≥ CH: | TH = CH + NCH | PsH = 0 |
| (13б) | TH | TH + PsH = CH | NCH = 0 | |
где 13a представляет собой «стандартное» соотношение твердости обычных учебников.
Пример: TH ≥ CH
Случай TH ≥ CH характерен почти для всех природных вод. Для иллюстрации возьмем пример воды C1.sol (кнопка Открыть ) со следующими параметрами:
| т | 10 ° С |
| pH | 7,34 |
| Алк | 2,50 мМ |
| Ca | 1,40 мМ |
| мг | 0.23 мМ |
| Na | 0,30 мМ |
| К | 0,05 мМ |
| Класс | 0,25 мМ |
| SO4 | 0,38 мМ |
| NO3 | 0,15 мМ |
Запустите пробу воды, нажав кнопку Start . Программа жалуется на ненулевой CBE, и мы устанавливаем точный баланс заряда путем настройки DIC (что снижает щелочность с 2.От 50 до 2,45 мэкв / л). Полученные значения твердости (как показано в столбце таблицы Output1 ):
Программа жалуется на ненулевой CBE, и мы устанавливаем точный баланс заряда путем настройки DIC (что снижает щелочность с 2.От 50 до 2,45 мэкв / л). Полученные значения твердости (как показано в столбце таблицы Output1 ):
| TH = 2,45 мэкв / л |
| CH = 3,26 мэкв / л |
Из разницы получаем: NCH = 0,81 мэкв / л. Псевдотвердости нет (PsH = 0). Общая жесткость определяется суммой Ca и Mg: TH = (2 × 1,40 + 2 × 0,23) мг-экв / л = 3,26 мг-экв / л — как показано на диаграмме выше.
Пример: TH
Мы используем тот же пример вода C1.sol и добавить 2 мМ NaOH (с кнопкой Reac ) .
Из-за добавления 2 мэкв / л сильного основания щелочность и, следовательно, CH увеличиваются на * 2 мэкв / л, при этом общая жесткость остается неизменной:
| CH = 4,45 мэкв / л |
| TH = 3,26 мэкв / л |
Здесь разница выражена псевдотвердостью: PsH = 1,19 мэкв / л. Нет NCH.
Нет NCH.
Значение PsH также можно рассчитать, подставив молярные концентрации входящей воды в 11 :
| (14) | PsH = (2.30 + 0,05) — (2 × 0,38 + 0,25 + 0,15) = 1,19 мэкв / л |
Обратите внимание, что Na также включает добавку 2 мМ NaOH : Na = (2,0 + 0,3) мэкв / л . Расчетное значение 14 явным образом показано как «Diff» на приведенной выше диаграмме.
Кальцитовые осадки. Из-за добавления 2 мМ NaOH вода становится перенасыщенной кальцитом. На нижнем графике показаны результаты при осаждении 1,37 мМ кальцита (столбец таблицы Output2 ):
| Канал | = | (4.45 — 2 × 1,37) мэкв / л | = | 1,71 мэкв / л |
| TH | = | (3,26 — 2 × 1,37) мэкв / л | = | 0,52 мэкв / л |
| PsH | = | CH — TH | = | 1,19 мг-экв / л (без изменений) |
Другие примеры
Далее мы добавляем один или два реагента в количестве 1 мМ в чистую воду (H 2 O). Результаты 20 расчетов приведены в таблице ниже; каждая строка относится к одному вычислению. Значения TH, CH, NCH и PsH приведены в последних столбцах.
Результаты 20 расчетов приведены в таблице ниже; каждая строка относится к одному вычислению. Значения TH, CH, NCH и PsH приведены в последних столбцах.
Примечание. В случаях, когда CaCO 3 (кальцит) становится перенасыщенным (SI> 0), добавляется дополнительная строка для отображения результатов после осаждения кальцита.
Таблица преобразования
Жесткость воды выражается в разных единицах:
| (15а) | Немецкий язык: | 1 ° д | = | 10 мг / л CaO |
| (15б) | Французский диплом: | 1 ° f | = | 10 мг / л CaCO 3 |
| (15c) | Английский градус (° Кларк): | 1 ° в. Д. | = | 10 мг CaCO 3 в 0.7 л |
| (15д) | 1 часть на миллион CaCO 3 (норма США): | 1 ° а | = | 1 мг / л CaCO 3 |
Эти единицы связаны между собой простыми правилами преобразования:
| частей на миллион CaCO 3 | ° d | ° F | ° в. д. д. | мэкв / л | ммоль / л | ||
| 1 часть на миллион CaCO 3 | = | 1 | 0.06 | 0,10 | 0,07 | 0,02 | 0,01 |
| 1 ° d | = | 17,8 | 1 | 1,78 | 1,25 | 0,357 | 0,178 |
| 1 ° | = | 10,0 | 0,56 | 1 | 0.70 | 0,2 | 0,1 |
| 1 ° в. Д. | = | 14,3 | 0,80 | 1,43 | 1 | 0,285 | 0,142 |
| 1 мэкв / л | = | 50,04 | 2,8 | 5 | 3,51 | 1 | 0. 5 5 |
| 1 ммоль / л | = | 100.09 | 5,6 | 10 | 7,02 | 2 | 1 |
Коэффициенты пересчета в этой таблице вытекают непосредственно из молярных масс карбоната кальция и оксида кальция:
| (16а) | CaCO 3 : | 100.09 г / моль | или | 1 мг / л CaCO 3 | = | 0,010 мМ |
| (16б) | CaO: | 56,08 г / моль | или | 10 мг / л CaO | = | 0,178 мМ |
Примечания и сноски
[последнее изменение: 15 декабря 2020 г.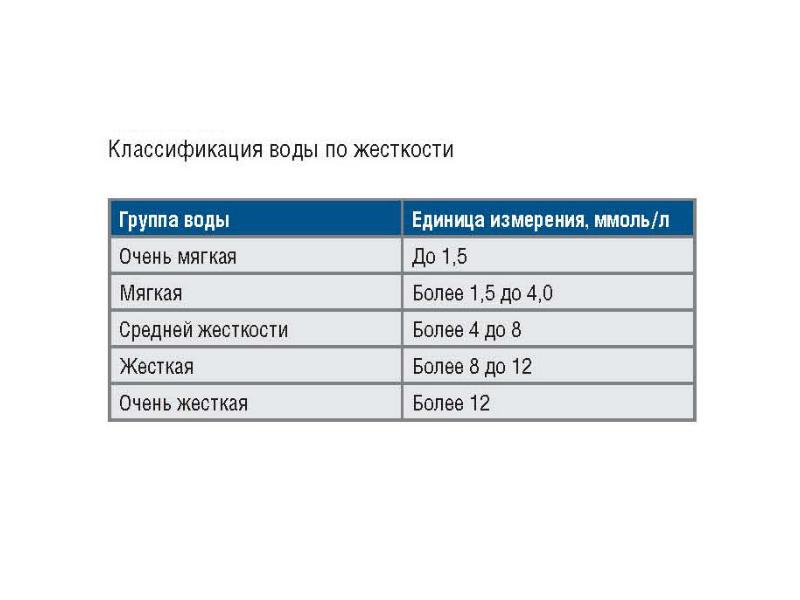 ]
]
Твердость
Накипные отложения — типичный показатель жесткости воды.
Жесткая вода (или жесткость воды) — это обычное качество воды, которая содержит растворенные соединения кальция и магния, а иногда и другие двухвалентные и трехвалентные металлические элементы.
Термин «жесткость» первоначально применялся к воде, в которой трудно было мыться, имея в виду свойство жесткой воды расходовать мыло. Жесткость предотвращает пенообразование мыла, вызывая образование нерастворимого творожного осадка в воде; твердость обычно вызывает накопление шкалы твердости (например, на сковороде).Растворенные соли кальция и магния в первую очередь вызывают образование накипи в трубах и водонагревателях и вызывают многочисленные проблемы в прачечной, на кухне и в ванной. Жесткость обычно выражается в зернах на галлон (или ppm) в эквиваленте карбоната кальция.
Что такое мягкая вода?
Мягкая вода определяется американскими национальными стандартами NSF / ANSI 44 и NSF / ANSI 330 как вода с жесткостью <1 грана на галлон (или <17,1 мг / л).
Симптомы жесткой воды включают:
- Жесткое, грязное белье
- Минеральные отложения на посуде и стеклянной посуде
- Большое количество мыла и необходимость в кондиционерах для белья
- Дополнительная работа по удалению мыльного творога с ванн и душевых кабин
- Высокие затраты на электроэнергию, возможно, из-за накопления накипи в трубах и на приборах
- Накипи в раковинах, ваннах, смесителях и бытовой технике
Щелкните здесь для получения национальных данных о наличии жесткой воды из США.С. Геологическая служба.
Обработка воды может улучшить проблемы с жесткостью.
Накипные отложения из-за накопления твердости влияют на приспособления и приборы, которые можно найти по всему дому или офису. По этой причине жесткость воды обычно решается путем обработки воды для всего дома или здания, а не только для конкретного крана.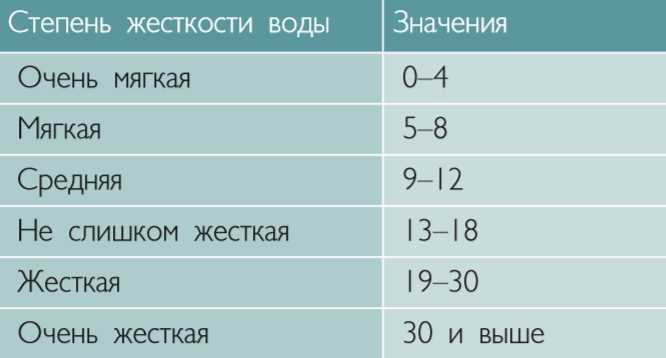 Минералы жесткости можно уменьшить в воде для всего дома, чтобы сделать ее «мягче», используя одно из следующих средств:
Минералы жесткости можно уменьшить в воде для всего дома, чтобы сделать ее «мягче», используя одно из следующих средств:
- Умягчение химическое — умягчение извести, горячее и холодное; лимонно-содовый умягчитель
- Смягчение мембранного разделения — нанофильтрация
- Катионообменное смягчение — неорганические, углеродсодержащие или органические основные обменники
Щелкните здесь, чтобы найти поставщика услуг по очистке воды, который может помочь.
Щелкните здесь, чтобы найти продукты, сертифицированные WQA для снижения твердости (сертифицированы по стандарту NSF / ANSI 44).
Общая жесткость воды связана с растворенными в ней минералами. Общий
твердость — это вводящий в заблуждение термин, который часто путают с карбонатной жесткостью или временной твердостью, которая на самом деле связана с
щелочность и относится к «буферной способности» воды (ее способности противостоять изменениям pH). Это означает, что если
карбонатная жесткость высока, тогда pH будет чрезвычайно стабильным или, альтернативно, если
карбонатная жесткость низкая, pH воды может легко колебаться. Термин «общая твердость» должен быть
заменен более простым термином: твердость. Это означает, что если
карбонатная жесткость высока, тогда pH будет чрезвычайно стабильным или, альтернативно, если
карбонатная жесткость низкая, pH воды может легко колебаться. Термин «общая твердость» должен быть
заменен более простым термином: твердость. Жесткость воды — это измерение количества ионов, потерявших два электрона. (двухвалентные катионы) растворены в тестируемой воде и, следовательно, относятся к общему количеству растворенных твердых веществ.Более двухвалентные катионы растворяется в воде тем «жестче» вода. Обычно наиболее распространенными двухвалентными катионами являются кальций и магний, однако другие двухвалентные катионы могут вносить вклад, включая железо, стронций, алюминий и марганец. Обычно другой двухвалентные катионы вносят незначительный вклад в измерение жесткости воды или не вносят заметных изменений в нее. Ручей или река твердость отражает геологию водосборного бассейна и иногда дает меру влияния человеческой деятельности на водораздел.Например, на участках, где поблизости есть действующие или заброшенные шахты, часто наблюдается более высокая концентрация ионов железа в вода, приводящая к очень высокой степени жесткости.  Жесткость воды может быть выражена во многих различных единицах, включая французские градусы, немецкие градусы. градусы, градусы Кларка, зерна на галлон, мг / л CaCO3 (карбонат кальция) и ppm (части на миллион). Общие преобразования находятся ниже: 1 ppm = 1 мг / л CaCO3Общее количество растворенных твердых веществ (TDS) относится к количеству всех неорганических твердых веществ, растворенных в воде.  Этот
означает, что он будет измерять ионы, которые влияют на жесткость воды, например, кальций, а также ионы, которые не влияют на жесткость воды, например, натрий. В
Измерение TDS лучше отражает общее содержание минералов в воде, чем измерение жесткости воды.Тем не мение,
в целях оценки жесткость воды можно приблизительно рассчитать, разделив значение ppm (частей на миллион) на
TDS на 10, что дает значение твердости с погрешностью всего 2-3 французских градуса. Измерения TDS также могут быть получены из
измерение относительной проводимости. Этот
означает, что он будет измерять ионы, которые влияют на жесткость воды, например, кальций, а также ионы, которые не влияют на жесткость воды, например, натрий. В
Измерение TDS лучше отражает общее содержание минералов в воде, чем измерение жесткости воды.Тем не мение,
в целях оценки жесткость воды можно приблизительно рассчитать, разделив значение ppm (частей на миллион) на
TDS на 10, что дает значение твердости с погрешностью всего 2-3 французских градуса. Измерения TDS также могут быть получены из
измерение относительной проводимости. Электропроводность аналогична измерениям TDS. Электропроводность — это мера способности вещество, проводящее электрический ток.Измерения проводимости предлагают быстрый и неразрушающий способ измерения ионов содержание в образце. Измерение проводимости производится электронным датчиком или измерителем в микро / миллисименсах на 1 метр. сантиметр или промилле. Электропроводность увеличивается с увеличением содержания ионов, а это означает, что в большинстве случаев она дает хорошее аппроксимация измерения TDS с использованием коэффициента преобразования 1 ppm = 2 мкСм / см. 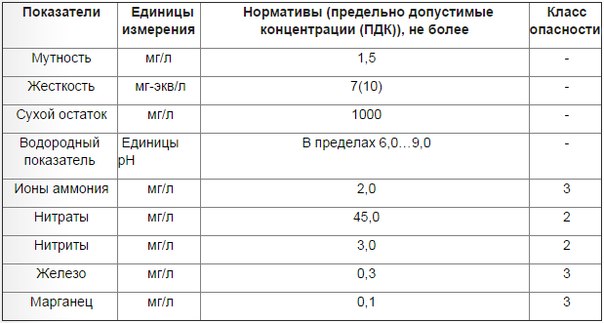 Электропроводность — это температура
чувствительны и обычно стандартизированы до 25 ° C.В то время как проводимость — удобный способ получить приближение
жесткость воды у него есть недостаток, заключающийся в объединении всех ионов при измерении, в том числе тех, которые не влияют на
жесткость воды. Это приближение твердости дает ошибку, аналогичную измерению TDS в 2-3 французских градуса твердости. Электропроводность — это температура
чувствительны и обычно стандартизированы до 25 ° C.В то время как проводимость — удобный способ получить приближение
жесткость воды у него есть недостаток, заключающийся в объединении всех ионов при измерении, в том числе тех, которые не влияют на
жесткость воды. Это приближение твердости дает ошибку, аналогичную измерению TDS в 2-3 французских градуса твердости. Можете ли вы измерить жесткость воды с помощью датчика проводимости или Датчик TDS? Да, но это зависит от точности, которую вы хотите измерение.В целом в следующей таблице описана жесткость воды, измеренная с помощью TDS, проводимости или жесткости. измерение. |
Наборы для испытания жесткости воды, тест-полоски и инструменты в Hach
Чаще всего твердость измеряют титрованием раствором ЭДТА. Титрование включает добавление небольшого количества раствора к пробе воды до тех пор, пока проба не изменит цвет. Вы можете титровать образец для определения общей жесткости с помощью бюретки или набора для анализа жесткой воды. Вы также можете измерить кальциевую жесткость отдельно от магниевой жесткости, регулируя pH и используя различные индикаторы.
Вы также можете измерить кальциевую жесткость отдельно от магниевой жесткости, регулируя pH и используя различные индикаторы.
Наборы для определения количества капель по Хачу для определения общей твердости используйте пипетку для добавления раствора ЭДТА к образцу. Комплект для испытания жесткой воды модели HA-71A, в котором используется индикатор ManVer, лучше всего подходит для проб естественной воды, особенно когда присутствует железо или марганец, или когда щелочность высока. Модели тестовых наборов 5-B, 5-EP и 5-EP / MG-L, в которых используется реагент UniVer, лучше всего подходят для промышленных образцов, которые могут иметь высокие концентрации металлов, таких как медь.Для отдельного измерения жесткости по кальцию и магнию доступны другие комплекты для проверки жесткости воды.
Наборы , использующие цифровой титратор , могут измерять концентрацию жесткости более точно, чем наборы для капельного титрования. Это связано с тем, что цифровой титратор дозирует раствор EDTA очень маленькими порциями. В наборах для анализа жесткой воды с использованием цифрового титратора используется индикатор ManVer.
Это связано с тем, что цифровой титратор дозирует раствор EDTA очень маленькими порциями. В наборах для анализа жесткой воды с использованием цифрового титратора используется индикатор ManVer.
Тест-полоски также доступны для измерения твердости.При использовании тест-полоски с жесткой водой на полоске появляется цвет, и полоска соответствует диаграмме. На диаграмме показаны цвета для концентраций 0, 25, 50, 120, 250 и 425 частей на миллион или 1, 1,5, 3,7, 15 и 25 галлонов на миллион. Используйте тест-полоски для жесткой воды, если общий диапазон жесткости достаточен. Не следует использовать тест-полоски, когда требуется точная концентрация жесткости.
Используйте колориметр или спектрофотометр , когда вам нужно измерить жесткость в очень мягкой воде, где ожидается, что концентрация будет менее 4 мг / л, как CaCO 3 .
Кальций также можно измерить с помощью ионоселективного электрода, такого как Radiometer ISE25Ca-9 Calcium Ion Selective Electrode (ISE) . Электрод — лучший метод для использования, когда цвет или помутнение образца мешают титрованию или колориметрическим методам.
Электрод — лучший метод для использования, когда цвет или помутнение образца мешают титрованию или колориметрическим методам.
Компания Hach также производит несколько онлайн-анализаторов для непрерывного контроля твердости, например, SP 510 Hardness Monitor и APA 6000 Analyzer .Эти инструменты могут активировать сигнализацию или насосы, когда концентрация жесткости достигает выбранных концентраций.
Как рассчитать жесткость воды
Вы слышали о термине «жесткая вода»? Что ж, вода содержит большое количество минералов, включая кальций и магний. Он также встречается во многих различных источниках воды по всему миру.
Хотя жесткая вода не вызывает болезней, она может вызвать различные проблемы в бытовой технике или на фабриках. Например, он может разрушить тяжелую технику, что приведет к дорогостоящему ремонту.Он даже образует меловые отложения на обогревателях или водопроводе, не позволяя мылу быстро образовывать пену.
Чтобы решить эту проблему, вам придется обработать воду. Но прежде чем приступить к поиску смягчителя воды; Давайте покажем вам, как рассчитать жесткость воды .
Что такое жесткость воды?
Жесткость воды можно определить как количество растворенных в воде минералов. Обычно жесткая вода содержит большое количество кальция и магния. Когда вы моете тело этой водой, вы можете почувствовать ее воздействие на вашу кожу.
В зависимости от количества минералов вы можете почувствовать пленчатый осадок на коже, особенно после мытья с мылом. Это ощущение возникает из-за того, что мыло вступает в реакцию с кальцием в воде, образуя «мыльную пену». В результате вам придется использовать дополнительное моющее средство или мыло с жесткой водой.
После мытья посуды в посудомоечной машине вы можете обнаружить на ней странные пятна. Эта пленка, также известная как остатки жесткой воды, имеет уродливый вид. Однако это не представляет опасности для вашего здоровья.
Как упоминалось ранее, дома и предприятия заботятся о жесткости воды. Ведь при нагревании вода образует густой осадок карбоната кальция или известкового налета.
Накипь может повредить оборудование, увеличить ваши счета за коммунальные услуги и повлиять на эффективность вашего водонагревателя. Он также может заблокировать вашу сантехнику и придать кофеварке некрасивый вид.
Чтобы вернуть кофеварке ее первоначальный вид, люди время от времени подбрасывают уксус в кастрюлю.Поскольку это вещество обладает кислотными свойствами, оно действует за счет накипи. Затем заряженные частицы движутся к молекулам воды, благодаря чему накипь легко смывается.
Есть ли преимущества у жесткой воды? Да, он предлагает жизненно важные минералы, которые выполняют функции в организме человека. Эксперты даже рекомендуют пить воду как способ увеличить содержание минералов в организме.
Что означает временная и постоянная твердость?
Временная жесткость воды
Эта форма жесткости возникает из-за присутствия в воде растворенных бикарбонатов кальция и натрия.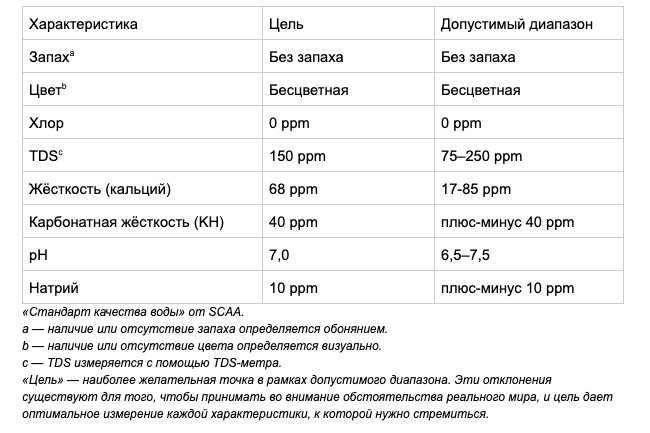 Вы можете уменьшить жесткость воды, добавив немного извести или гидроксида кальция (для смягчения извести).
Вы можете уменьшить жесткость воды, добавив немного извести или гидроксида кальция (для смягчения извести).
Постоянная жесткость воды
В отличие от упомянутого выше типа, эта жесткость требует специальной обработки из-за наличия в ней сульфатных и хлоридных ионов. Чтобы справиться с устойчивыми частицами, вам понадобится ионообменная смола или смягчитель воды .
Вы также можете описать постоянную жесткость как сумму кальциевой и магниевой жесткости воды.Если вы хотите узнать, как рассчитать жесткость воды, вам понадобится специальный тестовый набор.
Как работает калькулятор жесткой воды?
Как вы уже знаете, жесткость воды бывает двух видов — постоянной и временной. С помощью калькулятора жесткости воды вы можете определить общую постоянную жесткость. В калькуляторе используется следующая формула:
ОБЩАЯ ПОСТОЯННАЯ ТВЕРДОСТЬ = ЖЕСТКОСТЬ МАГНИЯ + ЖЕСТКОСТЬ КАЛЬЦИЯ
Кальций и магний представляют собой концентрацию обоих элементов, обозначенных как карбонат кальция.
Эти значения представляют собой молярную массу нескольких родственных соединений.
- CaC03 = 100,1 г / моль
- Ca2 + = 40, 1 г / моль
- Mg2 + = 24,3 г / моль
Отношение молярных масс может быть выражено как:
- MCaCo3 / MCa = 100, 1 / 40,1 = 2,5
- MCaCo3 / Mmg = 100,1 / 24,3 = 4,1
Это означает, что общую постоянную жесткость воды, равную CaCO3, можно определить по следующей формуле:
- (CaC03) = 2,5.(Ca2 +) + 4,1 (Mg2 +)
Итак, если вы ищете «как рассчитать формулу жесткости воды», вы можете использовать формулу выше .
Этапы определения карбонатной жесткости воды (CH)
Даже если полная жесткость в 1 зависит от количества катионов, она также может зависеть от количества анионов. Последний делит карбонатную жесткость / временную жесткость и постоянную жесткость.
- Общая жесткость TH = CH + NCH
Карбонатная жесткость зависит от щелочности:
- CH в мэкв / л = [Щелочь в мэкв / л]
- CH в ° dH = 809 × [Алк в мэкв.
 / L]
/ L]
Используя химический состав воды, щелочность и карбонатная жесткость имеют аналогичные значения.
- Карбонатная жесткость CH = Щелочность
С помощью программы вы можете рассчитать общую и карбонатную жесткость, отображая выходные таблицы, как показано ниже.
Как измерить жесткость воды?
Для измерения жесткости воды используется множество единиц измерения. К ним относятся зерна на галлон, миллиграммы кальция на литр, части на миллион. Вы можете использовать немецкую степень твердости; однако это устройство подходит только для аквариумов.
Чтобы определить жесткость, отправляйтесь в лабораторию для тестирования воды и возьмите образец воды.Затем преобразуйте результаты в меры жесткости воды. Например, 35 частей на миллион = 35 мг растворенных минералов на литр воды.
Как использовать мыло для определения степени жесткости в образце воды
Для этого теста вам понадобится небольшая бутылка с установленной крышкой и отметкой уровня воды.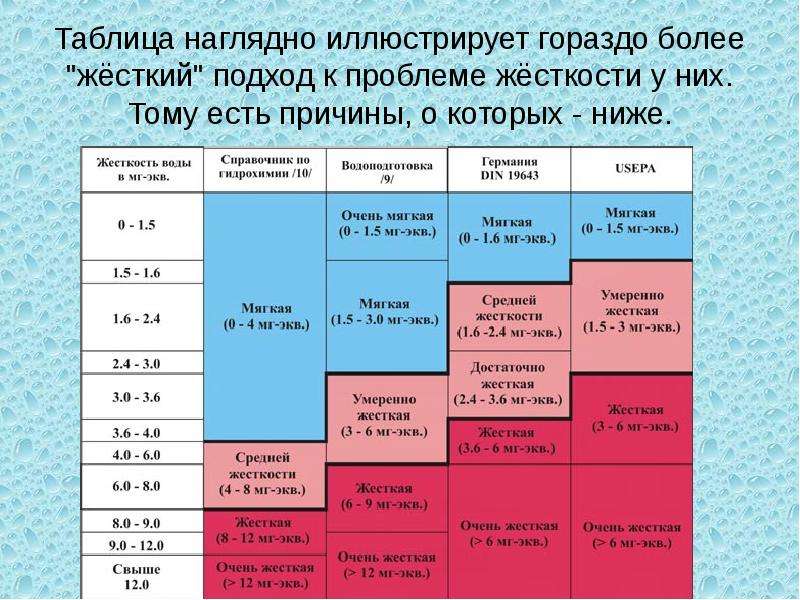 Вместо него вы можете использовать контейнер с маркировкой в комплекте для проверки жесткости воды. Вам также понадобится средство для мытья посуды и мерный стакан.
Вместо него вы можете использовать контейнер с маркировкой в комплекте для проверки жесткости воды. Вам также понадобится средство для мытья посуды и мерный стакан.
Теперь, когда вы знаете, как рассчитать жесткость воды в промилле, наполните бутылку (до отметки) водой.Налейте немного мыла и встряхните, чтобы образовались пузыри.
Если вам нужно добавить больше мыла, чтобы заметить пенообразование, это свидетельствует о большом количестве растворенных солей. Если вы используете меньше, значит, в воде мало минералов.
Хотя этот тест показывает жесткость воды, он не может дать точных показаний. Для точных тестов приобретите набор для проверки воды. Вы также можете получить эти предметы бесплатно или по доступным ценам.
Как измерить жесткость воды с помощью тестового набора
youtube.com/embed/AEz3SOkVW_8″ frameborder=»0″ allowfullscreen=»allowfullscreen»>Если вы хотите получить точное представление о жесткости воды в образце, используйте тестовые полоски со специальными подушечками.Вы даже можете использовать эти продукты, чтобы проверить, работает ли ваш дистиллятор или умягчитель воды.
Помимо этих устройств, некоторые приборы могут также давать показания жесткости воды. Теперь давайте посмотрим, как рассчитать жесткость воды по обоим параметрам.
Измерение жесткости воды с помощью инструментов
С помощью колориметра луч белого света проходит через оптический фильтр. Обычно экран посылает на фотоприемник свет определенного цвета для считывания.
Чтобы узнать количество цветного света, попадающего на образец, вам необходимо подтвердить разницу между количеством цветного света, испускаемого холостым и цветным образцом.
При использовании колориметрического теста вы обнаруживаете, что количество поглощенного света зависит от его концентрации. Вы даже можете заметить этот факт на счетчике.
Вы даже можете заметить этот факт на счетчике.
Измерение жесткости воды с помощью тест-полосок
Если вы хотите узнать, как измерить жесткость воды с помощью другого инструмента, подумайте о приобретении тест-полоски. Эти простые пластиковые изделия имеют на поверхности толстые подушечки. С помощью этих компонентов полоски могут обнаруживать определенный ион и создавать отчетливое изменение цвета.
Когда тест-полоска формирует цвет, это сравнивается с таблицей цветов. На этой распечатанной таблице вы найдете цветовые реакции при различных концентрациях. Вы можете получить показания, сравнив полоску с аналогичным цветом. Если вы не можете найти его, выберите оттенок, наиболее близкий к цвету на полоске.
Как рассчитать жесткость воды с помощью тест-полосок
Выберите источник воды
Для жесткости необработанной воды: Чтобы узнать, как измерить жесткость воды, поступающей в ваше место, поищите водопроводный кран. Вы также можете проверить источник, который не прошел через умягчитель или дистиллятор.
Вы также можете проверить источник, который не прошел через умягчитель или дистиллятор.
Избегайте сбора воды из садовой трубы, так как этот канал может содержать частицы, которые могут повлиять на ваши показания. Позвольте воде течь, пока она не достигнет стабильного уровня, так как это показывает, что вы набрали воду из внешнего источника.
Для очищенной воды с жесткостью : Чтобы проверить, хорошо ли работает ваш умягчитель, поищите источник воды, который простирается от умягчителя или наполнителя воды для всего дома.
Извлеките тест-полоску из упаковки. Убедитесь, что сенсорная панель не касается вашей кожи, так как любой контакт может повлиять на возможные показания.
Вставьте тест-полоску
Поместите тест-полоску в чистый стакан, наполненный пробой воды. Оставьте на 2 секунды или в соответствии с инструкциями производителя набора. Во избежание получения неточных результатов не оставляйте тест-полоску в воде на длительное время.
Вытяните полоску и встряхните, чтобы удалить лишнюю воду.Продолжайте махать, пока не исчезнут все капли воды. В целом убедитесь, что изделие немного влажно.
В горизонтальном положении удерживайте полоску 10–30 секунд. В течение этого времени на изделии могут появиться признаки химической реакции
Считайте жесткость воды
Чтобы узнать, как измерить жесткость воды с помощью полоски, сравните цвет его тестовой площадки с диаграммой жесткости воды на его упаковка. В большинстве случаев отображаемые цвета зависят от марки вашего набора для тестирования воды.
При правильном использовании ваша очищенная вода должна иметь показатель жесткости 0. Для неочищенной воды ожидайте более высокие значения до 425.
Wrap Up
Вода содержит растворенные минералы. Но когда они существуют в больших количествах, вода становится жесткой. К таким металлам относятся магний и кальций.
К основным типам жесткости относятся постоянная и временная жесткость воды. Для решения этих проблем вам могут потребоваться:
Для решения этих проблем вам могут потребоваться:
- Смягчитель воды или известь
- Для получения точных результатов вы можете использовать бутылку и тест мыла
- , приобретите доступный набор для проверки воды
Надеемся, вам понравилась наша статья, пожалуйста не стесняйтесь делиться с друзьями в социальных сетях.Если у вас есть какие-либо комментарии или вопросы, пожалуйста, оставьте их в свободном месте ниже.
Жесткость воды — обзор
5.2.2. Builder Systems
Сегодняшние строители почти полностью связаны с синтетическими поверхностно-активными веществами. Причина их использования заключается в улучшении или наращивании системы поверхностно-активных веществ для повышения эффективности очистки в широком диапазоне условий использования. К химическим веществам, которые классифицируются как добавки, относятся фосфаты, силикаты, карбонаты, этилендиаминтетраацетат (ЭДТА) и глюконаты.Строители действуют, связываясь с ионами металлов, помогая удалить их с подложки и способствуя их растворению или диспергированию. Таким образом, они помогают моющим средствам удалять и рассеивать твердые загрязнения.
Таким образом, они помогают моющим средствам удалять и рассеивать твердые загрязнения.
Добавки, смягчающие воду, очень важны. В мягкой воде мало или совсем нет свободных ионов жесткости, что помогает удерживать моющие средства и загрязнения в растворе, позволяя моющему средству лучше очищать и полоскать. Жесткая вода снижает моющие свойства и затрудняет смывание грязи. Кольцо для ванны — прекрасный пример того, как жесткая вода мешает процессу очистки.Ионы кальция и магния вступают в реакцию с ингредиентами чистящего раствора, образуя нерастворимую пленку, которую трудно смыть из ванны.
Есть проблемы с использованием некоторых сборщиков. Фосфаты, например, являются необходимыми питательными веществами для поддержания жизни растений. Однако слишком много фосфата в водной экосистеме может привести к эвтрофикации или отмиранию водной системы [13]. Свойства системы
Builder, связанные с производительностью, обычно включают следующее:
- •
Секвестрация жесткой воды.

- •
Дефлокуляция почвы.
- •
Обеспечивает щелочность.
- •
Диапазон pH буфера.
Идеальный строитель обладал бы всеми этими качествами. Однако комбинированные системы из двух или более ингредиентов вместе могут более эффективно выполнять эти функции. Кроме того, любая строительная или строительная комбинация должна быть стабильной в растворе. В наш век экологических и нормативных требований столь же важно, что любой строитель должен соответствовать жестким критериям безопасности для человека и экологической приемлемости.
У каждого типа построителя есть отличные друг от друга функциональные возможности. Некоторые строители предназначены для удаления почвы, а другие лучше умягчают воду. В любом случае, добавка предназначена для облегчения процесса очистки, обеспечивая лучшее полоскание и меньшее количество остатков.
Самая важная функция строителя — уменьшить влияние жесткости воды. Строители делают это, связывая или связывая ионы кальция и магния в воде, что в свободном состоянии может быть вредным для процесса очистки.Свободные ионы жесткости воды могут отрицательно повлиять на характеристики анионных поверхностно-активных веществ, заставляя их выделяться из раствора.
Строители делают это, связывая или связывая ионы кальция и магния в воде, что в свободном состоянии может быть вредным для процесса очистки.Свободные ионы жесткости воды могут отрицательно повлиять на характеристики анионных поверхностно-активных веществ, заставляя их выделяться из раствора.
Вторая по важности функция строителя — измельчение и диспергирование твердых частиц почвы. Это помогает удалить, рассредоточить и приостановить частицы почвы для эффективного удаления. Это очень важно для удаления с волокон глинистых загрязнений. Сложные фосфаты и силикатные добавки могут изменять адсорбцию моющего средства на субстрате и / или почве, а также действовать как суспендирующие агенты.
Строители должны обеспечивать безопасный уровень щелочности для обеспечения хорошей очистки. Буферизация — это способность поддерживать pH чистящего раствора в узком диапазоне, несмотря на добавление умеренных количеств кислот или основания. Некоторые составы обеспечивают как щелочность, так и буферную способность. В таких системах при уменьшении щелочности снижается способность модификатора действовать как буфер.
В таких системах при уменьшении щелочности снижается способность модификатора действовать как буфер.
5.2.2.1. Различные типы модификаторов
В зависимости от конкретного модификатора смягчение воды может осуществляться посредством хелатирования или связывания, ионного обмена или осаждения.По словам Уллы, использование строительных систем, которые действуют исключительно за счет атмосферных осадков (обычно на основе щелочей или монофосфатов), в Северной Америке устарело. Несмотря на то, что системы на основе карбоната натрия и содержащие полимерные соединения и / или смеси других модификаторов продолжают оставаться популярными [14]. Используемые системы нефосфатных модифицирующих добавок состоят из смеси модифицирующих и дополнительных модифицирующих добавок.
Уллах также указывает, что строители комплексообразующего типа можно разделить на два типа: те, которые содержат фосфор (фосфаты), и те, которые не содержат.Эти соединения действуют, хелатируя ионы жесткости воды, удерживая их в растворе и не позволяя им влиять на свойства поверхностно-активного вещества. С конца 1960-х годов использование фосфатных модификаторов, таких как триполифосфат натрия (STPP), все чаще подвергается критике из-за предполагаемого вклада в раннюю эвтрофикацию (непреднамеренное удобрение) водоемов [14].
С конца 1960-х годов использование фосфатных модификаторов, таких как триполифосфат натрия (STPP), все чаще подвергается критике из-за предполагаемого вклада в раннюю эвтрофикацию (непреднамеренное удобрение) водоемов [14].
Фосфаты включают пирофосфаты, триполифосфаты и метафосфаты. Фосфаты обладают необычной способностью пептизировать и суспендировать определенные глины, пигменты и другие мелкодисперсные твердые вещества в водных растворах.Отчасти это связано с улавливающей способностью фосфатов. В то время как значительные исследования были посвящены разработке строительных материалов без фосфатов, лишь немногие из них были коммерциализированы.
EDTA — один из наиболее распространенных модифицирующих добавок, который особенно хорошо удаляет кальций и магний, способствуя смягчению воды. Благодаря своей эффективности ЭДТА содержится в широком спектре промышленных и потребительских товаров. ЭДТА захватывает ионы металлов за счет хелатирования и образует очень прочные комплексы с металлами, что затрудняет отделение ионов металлов от потока воды. Таким образом, могут возникнуть проблемы с высоким содержанием металлов в сточных водах из-за EDTA.
Таким образом, могут возникнуть проблемы с высоким содержанием металлов в сточных водах из-за EDTA.
5.2.2.2. Полимерные системы
Водорастворимые полимеры используются в сочетании с другими компонентами моющих средств для оптимальной очистки и затрат. Эти полимеры предназначены для использования при очистке с высокими нагрузками на почву, в условиях жесткой воды и умеренной температуры. Они предназначены для облегчения очистки за счет диспергирования твердых частиц, предотвращения повторного осаждения загрязнений и связывания минеральных ионов, таких как ионы кальция и магния.Например, полиакриловые кислоты, полиакрилаты, сополимеры акриловой и малеиновой кислоты — вот некоторые типы полимеров, используемые для чистки ковров.
Кроме того, в составах для чистки ковров используются полимерные материалы, такие как смола стирол / малеиновый ангидрид (SMA), сополимеры акрилата, фторсодержащие акрилаты и т. Д., Для придания защитных свойств от повторного загрязнения и окрашивания.
5.2.2.3. Ароматизаторы
Ароматы добавляются к средствам для чистки ковров, чтобы придать им приятный и характерный аромат.Ароматические материалы используются для выполнения трех функций независимо от запаха. Они нейтрализуют химический запах продукта и запах грязи в восстановленном чистящем растворе. Они придают приятный запах ковровым тканям и окружающей атмосфере, тем самым усиливая чистоту продукта. Кроме того, аромат отличает продукт, чтобы сформировать характер этого продукта.
5.2.2.4. Растворители
Растворители удаляют жир и масло и улучшают общие очищающие свойства состава для чистки ковров.Кроме того, некоторые типы растворителей используются в рецептурах для получения прозрачных стабильных продуктов. Однако сегодня средства для чистки ковров для дома разработаны с учетом нормативных требований и требований охраны окружающей среды. Из-за этих требований, по опыту автора, включение достаточного количества растворителя для обеспечения эффективности и действенности может быть трудным, и все больше и больше составов основаны на системах поверхностно-активных веществ.
5.2.2.5. Источник воды
Вода — самый распространенный ингредиент, используемый в средствах для чистки ковров на водной основе.Тип и количество примесей, содержащихся в воде, различаются в зависимости от источника (озеро, река или колодец) и географического района. Городская вода содержит растворенные ионы кальция, магния, железа и других материалов, которые выше определенного уровня считаются «жесткой водой». Жесткость муниципальной воды варьируется и может составлять от 50 до более 250 частей на миллион (ppm). Кроме того, pH воды может варьироваться от примерно 6,5 или выше, если вода поступает из колодцев и водохранилищ.
При разработке чистящих средств важно знать качество воды.Хотя агенты обычно добавляются для противодействия ионам жесткости воды, они могут быть частично исчерпаны в процессе смешивания за счет реакции с ионами жесткости необработанной воды. В идеале вода, используемая для приготовления чистящих средств, должна быть обработана для удаления ионов жесткости и следов металлов.
Набор для проверки общей жесткости воды AQUAX®
Что такое жесткость воды?
Вода является хорошим растворителем и легко улавливает загрязнения. Чистая вода без вкуса, цвета и запаха, как ее часто называют универсальным растворителем.Когда вода движется через почву и камни, она растворяет очень небольшое количество минералов и удерживает их в растворе. Растворенные в воде кальций и магний — два самых распространенных минерала, которые делают воду «жесткой». Степень жесткости увеличивается по мере увеличения содержания кальция и магния и связана с концентрацией многовалентных катионов, растворенных в воде.
Почему важна жесткость воды?
Многие промышленные и бытовые водопользователи обеспокоены жесткостью воды.Возможно, вы почувствовали воздействие жесткой воды буквально во время последнего мытья рук. В зависимости от жесткости воды после использования мыла для стирки вы могли почувствовать, что на ваших руках осталась пленка остатков. В жесткой воде мыло реагирует с кальцием (который в жесткой воде относительно высок), образуя «мыльную пену». При использовании жесткой воды необходимо больше мыла или моющего средства, чтобы вымыть вещи, будь то руки, волосы или белье.
В жесткой воде мыло реагирует с кальцием (который в жесткой воде относительно высок), образуя «мыльную пену». При использовании жесткой воды необходимо больше мыла или моющего средства, чтобы вымыть вещи, будь то руки, волосы или белье.
Вы также можете заметить пятна или пленку на стеклянной посуде после ее выгрузки в посудомоечной машине.Это более твердый остаток воды, не опасный, но неприглядный. Когда жесткая вода нагревается, например, в домашнем водонагревателе, могут образовываться твердые отложения карбоната кальция. Эти накипи могут сократить срок службы оборудования, повысить затраты на нагрев воды, снизить эффективность электрических водонагревателей и забить трубы. Жесткая вода может даже сократить срок службы тканей и одежды.
Как показано на этом изображении внутренней части трубы для подачи воды, длительное движение жесткой воды по трубе может привести к так называемому накоплению накипи.Так же, как в человеческом теле, где внутренний диаметр кровеносных сосудов может уменьшаться из-за накопления холестерина, водопроводные трубы могут постепенно закрываться, что приводит к меньшему движению воды по трубе и снижению давления воды.
Вот почему качество и жесткость воды очень важны как в промышленности, так и в повседневной жизни! Это важный параметр, за которым нужно постоянно следить.
Меры жесткости воды
Общие правила классификации вод:
| Немецкая твердость d ºH | Твердость по французскому шкале f ºH | CaCO 3 (мг / л или ppm) Карбонат кальция | Оценка |
| 0–4 | 0–7 | 0–71 | Очень мягкий |
| 4–12 | 7–21 | 71–160 | Средняя твердость |
| 12–17 | 21–30 | 160–213 | Жесткий |
| > 17 | более 30 | более 213 | Очень жесткий |
ПРИМЕЧАНИЕ: Другие организации могут использовать другие классификации.
Измерение общей жесткости воды с помощью тестового набора AQUAX ®
Жесткость воды можно приблизительно определить с помощью набора для измерения общей жесткости воды AQUAX ® .
AQUAX ® был разработан на основе одного реагента (буферный раствор для определения жесткости) для простого, быстрого и правильного определения качества воды титриметрическим методом. Простое приложение для поиска и просмотра обеспечивает надежные результаты в течение нескольких секунд.
МЕТОД ИСПЫТАНИЯ
- Наполните контейнер для теста водой для анализа, встряхните два или три раза и слейте.Залейте 5 мл воды для анализа.
- Добавьте 1 каплю буферного раствора индикатора жесткости и встряхните контейнер для теста.
- a) Если цвет пробы воды становится зеленовато-голубоватым, жесткость отсутствует. В этом случае завершите эксперимент и укажите его как «Нулевая жесткость».

- б) Если образец воды имеет какую-либо жесткость, цвет станет розово-красноватым.
- Если цвет становится розово-красноватым, продолжайте добавлять индикатор жесткости Buffer Solution по каплям, встряхивая после каждой капли и наблюдая за цветом.
- Когда цвет становится зелено-голубоватым, эксперимент завершается.
РЕЗУЛЬТАТ: Количество капель, потраченных во время эксперимента, записывается как величина жесткости в немецких единицах (° dH).
1 капля = 1 немецкая жесткость (° dH).
Коэффициенты пересчета твердости
1 Немецкая жесткость (° dH) = 1,78 Французская жесткость (° fH) = 17,8 мг / л CaCO 3
Характеристики AQUAX ®
Поставляется с реагентом на 50 мл (буферный раствор для определения жесткости) и тестовым контейнером в коробке.
- Широкие области применения: все отрасли, такие как текстильная, сельское хозяйство, прачечная, аквариум, рыбалка, дом и все области, где важна жесткость воды
- 100 капель в одном реагенте 50 мл (буферный раствор для определения жесткости)
- Измерение твердости по немецкому языку (легко конвертируется во французскую твердость — см.


 / L]
/ L]

