Снижение щелочности воды | Гидрокарбонаты в воде, как убрать
Щелочность бывает нескольких типов: карбонатная, бикарбонатная, гидратная. Уровень щелочности характеризуется количеством кислоты, необходимой для ее снижения. Если брать воду из естественных источников, подземных или поверхностных, щелочность в ней зависит от присутствия гидрокарбонатов кальция и магния.
Повышенная щелочность воды, особенно той, что используется в отопительных системах, плохо сказывается на оборудовании, качестве изготовленной из нее продукции. Под высокой щелочностью понимают повышенную концентрацию в воде ионов, вступающих в связь с сильной кислотой. Особенно огорчает большое содержание карбонатов. Щелочность воды – это сумма гидроксильных ионов, а также слабокислотных анионов, что присутствуют в воде. Они могут быть угольными, органическими, бикарбонатными и карбонатными.
Методы снижения щелочности:
- Обратный осмос, во время которого значительно снижается минерализация воды, уменьшается содержание щелочных анионов. Самый эффективный метод. Его можно считать универсальным, но установки обратного осмоса должны использоваться только отличного качества. При применении подобных установок, не обладающих достаточной технологичностью, а также имеющих несовершенную конструкцию, могут возрасти расходы на эксплуатацию оборудования, его обслуживание. Мембранные элементы будут быстро выходить из строя.
- Катионирование воды с применением слабокислотного катионита, имеющего водородную форму. Помимо уменьшения кислотности совершается неполная деминерализация, отклонение рН в сторону кислотности. Также может нормализоваться минеральный состав, точнее, содержание отдельных его соединений.

Назад в раздел
Питьевая щелочная вода — насколько благотворно ее влияние на организм? Обзор литературы | #06/19
В последнее время появилось множество публикаций на тему питания, которое помогает живому организму поддерживать кислотно-щелочное равновесие, не позволяя ему сдвигаться в кислую сторону [1, 2]. Такое питание включает в себя как рацион, насыщенный овощами и фруктами, так и употребление щелочной воды.
Кислотно-щелочной баланс внутренней среды организма поддерживается в достаточно жестких границах на уровне pH артериальной крови от 7,26 до 7,45 буферными системами организма [3], и принято считать, что он изменяется только при тяжелых заболеваниях. Однако анализ кислотно-щелочного равновесия крови, как правило, проводился у пациентов с выраженной патологией и мало изучался у практически здоровых людей, подверженных негативному влиянию экологии, стрессам, изменению в питании и проч. В настоящее время отрабатываются более чувствительные методы и модели, которые, возможно, помогут понять более тонкие, но весьма существенные для здоровья колебания pH [4, 5].
Есть исследование, убедительно доказывающее, что не только тяжелые состояния здоровья, но и условия работы в современной промышленности достоверно сдвигают традиционные показатели буферной системы крови (pH, РаCO2, РаO2 крови и HCO в плазме) у рабочих завода по производству пластмасс [6]. О более тонких изменениях кислотно-щелочного равновесия в связи с эволюцией питания людей в историческом разрезе изложено также в European Journal of Nutrition в 2001 г. [7]. Там же указано, что «во время высокоинтенсивной активности ацидоз ответственен за усталость и истощение рабочих мышц. Введение бикарбонатной добавки перед тренировкой улучшало показатели, задерживая начало усталости». Кислотно-щелочное равновесие зависит от питания перед высокоинтенсивной тренировкой. Низкое употребление углеводов перед тренировкой приводит после интенсивной нагрузки к его сдвигу в кислую сторону [8, 9].
Таким образом, роль питания в поддержании кислотно-щелочного баланса подтверждена и продолжает изучаться, и немалую долю в рационе составляет вода, оказывающая значимое влияние на здоровье наряду с пищей. В литературе накопилось немало данных о благоприятном воздействии на здоровье употребления питьевой щелочной воды, являющейся основой для коррекции кислотно-щелочного равновесия на фоне привычного для человека питания. Изучалось ее влияние на общее оздоровление, уровень глюкозы в крови, массу тела, восстановление спортсменов после напряженных тренировок и проч., что будет отдельно рассмотрено ниже.
Материалы и методы исследования
Были проанализированы рандомизированные клинические исследования, а также группы нерандомизированных исследований.
Результаты и обсуждения
Питьевая вода во всех странах регулируется по показателю pH, однако допустимый диапазон колебаний достаточно широкий. В Российской Федерации допустимыми параметрами для питьевой воды является pH в диапазоне 6–9 [14], охватывая диапазон от слабокислой до щелочной реакции. Питьевая вода с водородным показателем 8–9 является щелочной, находясь в нормируемых параметрах для ежедневного потребления.
Одним из самых спорных вопросов, возникающих при рассмотрении пользы питьевой щелочной воды, является сомнение в том, что она может полностью нейтрализоваться кислой средой желудка. Действительно, на первый взгляд этот вопрос очевиден, и есть предположение, что щелочная среда будет полностью инактивирована желудочным соком, потеряв свои полезные свойства.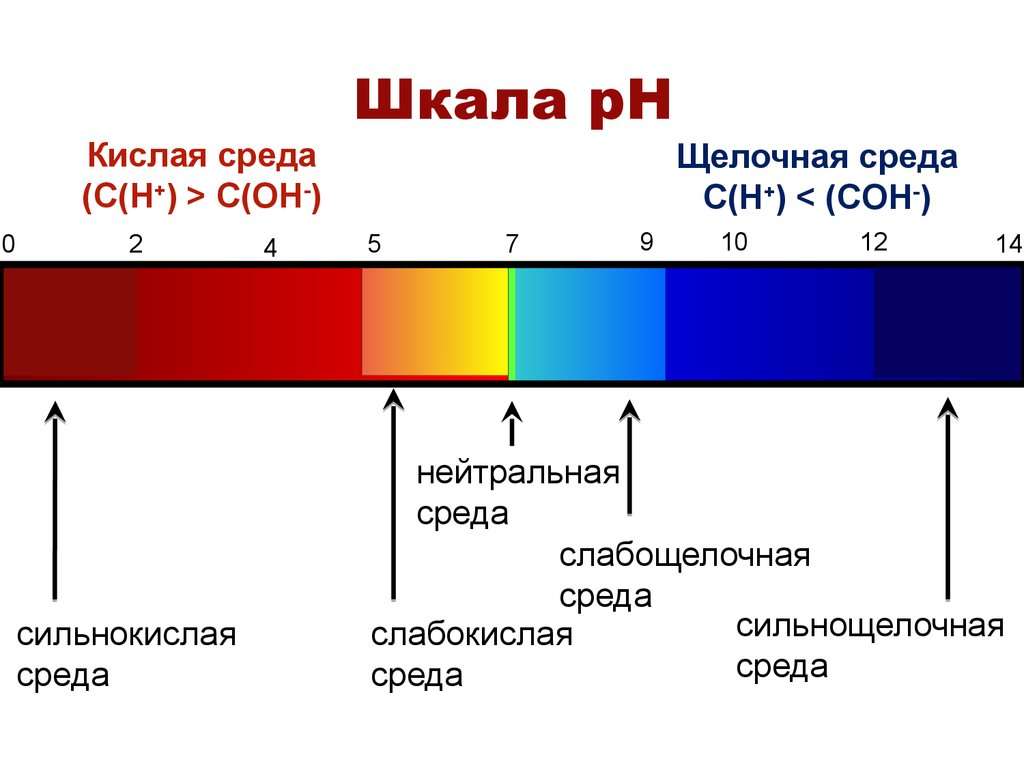
Для понимания степени и времени контакта щелочной воды с кислотностью желудка необходимо рассмотреть особенности эвакуации жидкости и пищи из желудка. Методы изучения особенности эвакуации содержимого желудка включают методы взятия проб желудочно-кишечного тракта [15–18], сцинтиграфию [19, 20], фармакокинетический анализ маркерных веществ [21] и магнитно-резонансную томографию (МРТ) [22, 23].
Впоследствии феномен Вальдейера был неоднократно описан другими авторами [25, 26] и в 70-х годах прошлого столетия был окончательно подтвержден [27, 28]. В 2007 и 2015 гг. феномен быстрой эвакуации воды (в течение 10 мин) из желудка был подтвержден с помощью математических моделей [29, 30].
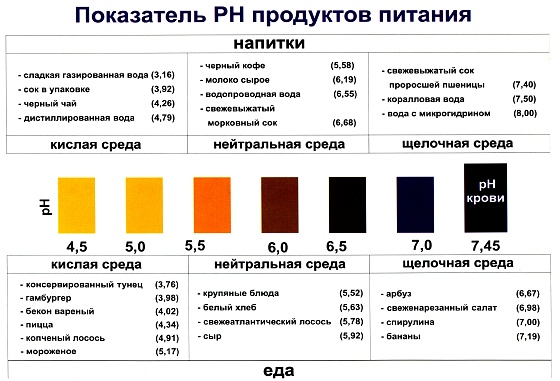 Более всего задерживает эвакуацию гомогенная нежирная пища, с которой происходит смешивание жидкости в желудке.
Более всего задерживает эвакуацию гомогенная нежирная пища, с которой происходит смешивание жидкости в желудке.На скорость эвакуации воды влияет также ее температура — прохладные напитки (5–20 °C) проходят из желудка в двенадцатиперстную кишку быстрее, чем теплые (25–40 °C) [32, 33]. Следует отметить, что все исследования проводились на объемах 250–350 мл, то есть эвакуаторная функция желудка при употреблении больших объемов пищи не изучалась, вода также выпивалась в количестве 250 мл.
Несмотря на то, что вопрос особенностей эвакуации воды из желудка был достаточно хорошо изучен и подтвержден, он известен только определенному кругу исследователей и широко не обсуждается в кругах практических врачей. Хотя именно этот феномен помог бы понять механизм всасывания и расщепления некоторых лекарств и жидкостей, долгое соприкосновение которых с кислой средой желудка было бы нежелательно.
Воздействие на организм человека щелочной воды, полученной электролизом, изучалось отдельными авторами как в моделях на животных, так и у людей. Общеоздоровительный эффект от постоянного употребления такой воды рассматривался, в частности, с точки зрения воздействия на окислительные процессы, вызывающие обширное повреждение биологических макромолекул и ведущие к различным заболеваниям, старению и мутациям. В частности, были рассмотрены механизмы защиты от окисления и повреждения РНК, ДНК и белков как in vitro [34–37], так и in vivo у лабораторных крыс [38].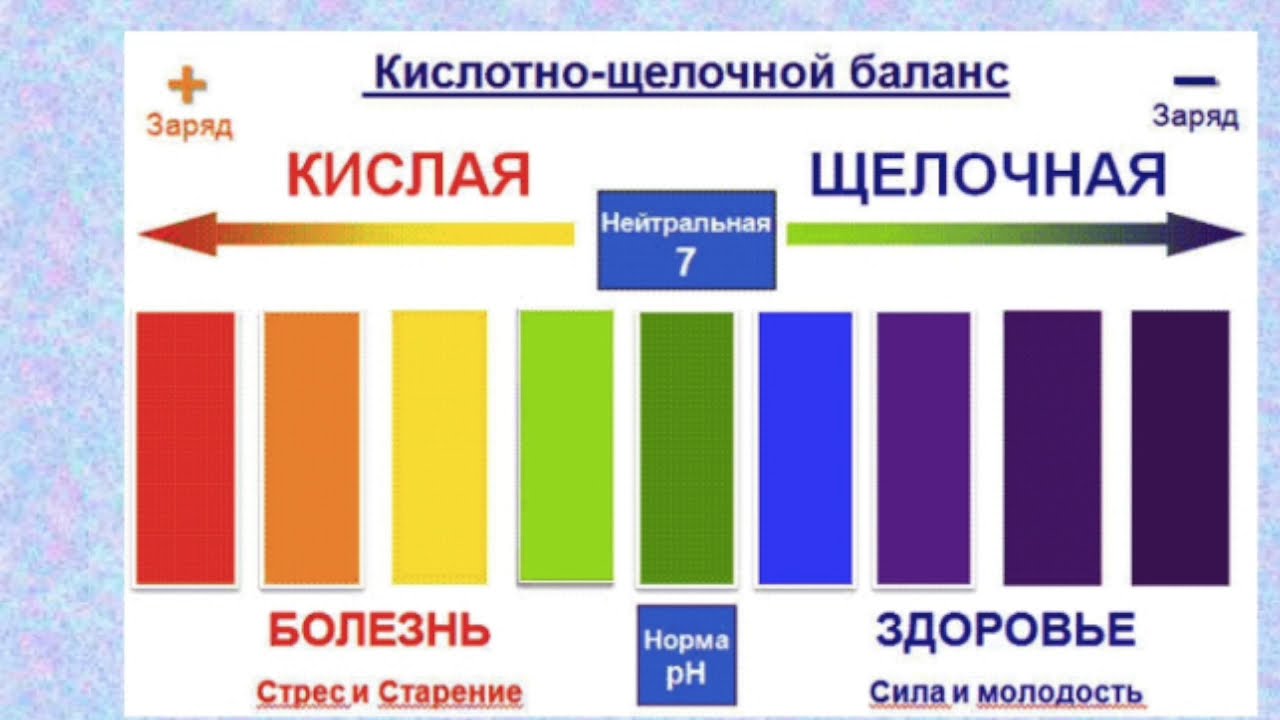 Предполагалось, что щелочная вода является идеальным поглотителем активного кислорода, являющегося одним из мощных повреждающих факторов в живых системах. Результаты исследований подтвердили данный тезис. Все эти исследования установили, что щелочная вода имела тенденцию подавлять одноцепочечный разрыв ДНК, РНК и защищать белок от воздействия окислительного стресса. Доказано также, что щелочная вода повышает активность ключевого детоксифицирующего фермента в организме, супероксиддисмутазы, который является основной защитой от повреждения свободными радикалами [34, 35].
Предполагалось, что щелочная вода является идеальным поглотителем активного кислорода, являющегося одним из мощных повреждающих факторов в живых системах. Результаты исследований подтвердили данный тезис. Все эти исследования установили, что щелочная вода имела тенденцию подавлять одноцепочечный разрыв ДНК, РНК и защищать белок от воздействия окислительного стресса. Доказано также, что щелочная вода повышает активность ключевого детоксифицирующего фермента в организме, супероксиддисмутазы, который является основной защитой от повреждения свободными радикалами [34, 35].
Вода с щелочным диапазоном (pH 8,5–9,5) хорошо продемонстрировала свое антиоксидантное действие у пациентов, находящихся на диализе. K. C. Huang и соавт. изучили активные формы кислорода в плазме этих пациентов и обнаружили, что такая вода снижает уровень пероксида, повышенный гемодиализом, и минимизирует маркеры воспаления (С-реактивный белок и интерлейкин-6) после 1 месяца употребления. Эти данные показывают, что сердечно-сосудистые осложнения (инсульт и сердечный приступ) у пациентов, находящихся на гемодиализе, могут быть предотвращены или отсрочены с помощью такого безобидного питья [39]. Причем по активности и результатам анализов употребление щелочной воды у этой группы пациентов сравнимо с действием инъекционного витамина С, но, в отличие от последнего, без риска образования оксалатов [40]. В этой же статье отмечено, что шестимесячный прием щелочной воды увеличил гематокрит и уменьшил количество цитокинов, обеспечивающих мобилизацию воспалительного ответа.
Известно, что именно свободнорадикальное окисление приводит к развитию многих возрастных болезней, поэтому антиоксиданты могут быть полезными для смягчения разрушительного действия старения и, возможно, для его замедления. G. Fernandes из Университета Техаса сообщил, что различные виды лабораторных мышей, получавших щелочную воду с рождения, живут на 20–50% дольше контрольной группы, употреблявшей водопроводную воду. Он также обнаружил снижение уровня пероксида в сыворотке опытных мышей по сравнению с контрольными [41]. Исследование, проведенное на нематодах, у которых в качестве водной среды использовалась щелочная вода, показало, что она значительно продлила продолжительность жизни червей, что было интерпретировано как проявление поглощающего действия активных форм кислорода [42].
Исследование, проведенное на нематодах, у которых в качестве водной среды использовалась щелочная вода, показало, что она значительно продлила продолжительность жизни червей, что было интерпретировано как проявление поглощающего действия активных форм кислорода [42].
Оздоровительный эффект при приеме щелочной воды зарегистрирован и описан у людей в исследовании Н. В. Воробьевой (МГУ им. М. В. Ломоносова) при изучении микрофлоры кишечника. Отмечалась стимуляция роста нормальной анаэробной флоры. Положительное воздействие трактовалось автором как улучшение среды обитания и благоприятного микроэкологического фона для роста аутомикрофлоры [43].
Исследование, проведенное в Китае в 2001 г. с людьми, продемонстрировало, что прием щелочной воды на протяжении от 3 до 6 месяцев снижал вплоть до нормальных значений гиперлипидемию, уровень глюкозы крови при сахарном диабете 2 типа легкой степени и регулировал уровень артериального давления [44]. Аналогичные результаты с регуляцией сахара крови были получены и в других исследованиях. Другое исследование 2006 г., проведенное на лабораторных крысах с экспериментальным диабетом, подтвердило данные результаты [45]. Через 12 недель употребления щелочной воды снижались уровни холестерина, триглицеридов и сахара в крови.
Поскольку сахарный диабет 2 типа является достаточно актуальной проблемой в современном обществе, ему уделяется много внимания различными исследователеми. Интересные результаты были получены на людях, больных диабетом 2 типа, которые были разбиты на группы и получали воду с различным pH (7,0; 8,0; 9,5 и 11,5) в течение 14 дней. Было обнаружено, что сахароснижающее свойство проявляет вода с pH 9,5 и 11,5, тогда как более низкие значения не оказывают статистически достоверного влияния на глюкозу в крови [46]. Авторы также отмечают, что наряду с сахароснижающим эффектом щелочная вода проявляет выраженное антиоксидантное действие, которое необходимо больным сахарным диабетом, а также выраженный детоксикационный эффект, проявляющийся в учащенном мочеиспускании. Корейское исследование, проведенное на мышах с диабетом, подтвердило, что питье щелочной воды значительно снижало концентрацию глюкозы в крови и улучшало толерантность к глюкозе [47]. Однако не было выявлено воздействия на уровень инсулина. Еще два исследования подтвердили не только способствование снижению глюкозы в крови и нормализации толерантности к глюкозе, но и лучшее сохранение β-клеток поджелудочной железы, активно разрушающихся при прогрессировании данного заболевания [48, 49].
Корейское исследование, проведенное на мышах с диабетом, подтвердило, что питье щелочной воды значительно снижало концентрацию глюкозы в крови и улучшало толерантность к глюкозе [47]. Однако не было выявлено воздействия на уровень инсулина. Еще два исследования подтвердили не только способствование снижению глюкозы в крови и нормализации толерантности к глюкозе, но и лучшее сохранение β-клеток поджелудочной железы, активно разрушающихся при прогрессировании данного заболевания [48, 49].
Исследования, посвященные действию щелочной воды на организм, были также проведены среди спортсменов и среди людей, получавших интенсивные физические нагрузки. Предполагается, что интенсивные физические нагрузки провоцируют окислительный стресс в организме [50]. Дегидратация после тренировок также провоцирует повышение уровня малонового альдегида, являющегося одним из маркеров окислительного стресса [51]. К окислению весьма чувствительны эритроциты. Насыщенный железом гемоглобин разлагается, выделяя супероксид [49, 52]. Когда активные формы кислорода инициируют перекисное окисление липидных мембран, белки клеточных мембран часто становятся сшитыми, а эритроциты становятся более жесткими с меньшей подвижностью [53]. Эти механизмы изменяют свойства эритроцитов, в том числе снижают текучесть крови и повышают агрегацию ее клеток, что приводит к увеличению вязкости крови и нарушению кровотока [54]. Аналогичные изменения под действием окислителей происходят и с тромбоцитами [55]. Агрегацию тромбоцитов усиливает и финибриноген, испытывающий действие окислительного стресса [56]. Поэтому одним из показателей выраженного окислительного стресса у спортсменов можно рассматривать повышение вязкости крови, которую усугубляет дегидратация после интенсивных тренировок.
Быстрое восстановление после интенсивных физических нагрузок является актуальной проблемой в спортивной медицине. J. Weidman и соавт. провели двойное слепое рандомизированное исследование для сравнения эффективности регидратации после тренировок с применением стандартной питьевой и щелочной воды (pH 9,5), полученной электролизом, в котором изучали показатели вязкости крови [57]. В этом исследовании была обнаружена значительная разница в вязкости цельной крови при оценке употребления воды с высоким pH по сравнению со стандартной очищенной водой во время фазы восстановления (120 мин) после интенсивной дегидратации, вызванной физической нагрузкой. Авторы объясняют полученные результаты нейтрализацией окислительных процессов, выявленных после интенсивных физических нагрузок в организме спортсменов. Исследование, проведенное с тремя видами воды: минеральной (pH 6,1), щелочной с низким содержанием минералов (pH 8) и обычной питьевой водой, также выявило лучшую регидратацию после высокоинтенсивных интервальных тренировок с улучшением утилизации лактата при употреблении после нагрузок щелочной воды с низким содержанием минералов [58].
В этом исследовании была обнаружена значительная разница в вязкости цельной крови при оценке употребления воды с высоким pH по сравнению со стандартной очищенной водой во время фазы восстановления (120 мин) после интенсивной дегидратации, вызванной физической нагрузкой. Авторы объясняют полученные результаты нейтрализацией окислительных процессов, выявленных после интенсивных физических нагрузок в организме спортсменов. Исследование, проведенное с тремя видами воды: минеральной (pH 6,1), щелочной с низким содержанием минералов (pH 8) и обычной питьевой водой, также выявило лучшую регидратацию после высокоинтенсивных интервальных тренировок с улучшением утилизации лактата при употреблении после нагрузок щелочной воды с низким содержанием минералов [58].
В другом исследовании D. P. Heil продемонстрировал более быструю и лучшую регидратацию с бутылочной щелочной водой (pH 10), чем со стандартной питьевой водой у десяти велосипедистов мужского пола. Маркерами регидратации были удельный вес мочи, диурез, концентрация сывороточного белка и восстановление водного баланса [59]. Бикарбонатная бутылочная щелочная вода с микроэлементами (pH 9,1) показала также лучшие восстановительные свойства по сравнению с питьевой водой и у спортсменов боевых искусств после ограничения воды для быстрой потери веса перед соревнованиями [60]. Перечисленные исследования демонстрируют, что лучшие восстановительные свойства показывает вода со щелочным pH по сравнению с нейтральной питьевой водой, независимо от того, получена она электролизом или это бутылочный вариант.
Выводы
Таким образом, вода с pH 9–10 может рассматриваться как дополнительный фактор оздоровления. Растущий объем научных исследований не выявил негативных отрицательных воздействий на организм. Из рассмотренных публикаций очевидно, что употребление щелочной воды может быть дополнительной антиоксидантной поддержкой, благоприятно сказывается на состоянии здоровья при диабете и гиперлипидемии и может улучшать реологию крови в случае, когда она нарушена из-за интенсивных физических нагрузок. Применение щелочной воды в спорте для более активного восстановления после тренировок может дать дополнительный безопасный инструмент сохранения здоровья спортсменов.
Применение щелочной воды в спорте для более активного восстановления после тренировок может дать дополнительный безопасный инструмент сохранения здоровья спортсменов.
Литературные данные, приведенные в обзоре, также могут помочь выработать рекомендации по приему щелочной воды для максимального сохранения ее полезных свойств. Особенности эвакуаторной функции желудка при употреблении пищи объемом до 250 мл позволяют большей ее части не смешиваться с его содержимым. Однако это касается не всего объема выпитой воды. Часть ее все-таки смешивается, особенно если пища является гомогенной и полужидкой. Наиболее полно сохранение свойств с наибольшей вероятностью произойдет при употреблении щелочной воды натощак или между приемами пищи. Следует также принимать во внимание, что исследования касались объема жидкости до 250 мл. Каким образом эвакуируются из желудка большие объемы воды, на сегодняшний день остается не изученным.
В заключение следует отметить, что сохраняется высокая актуальность исследований воздействия щелочной воды на здоровье, поскольку есть перспективы дополнительного безопасного алиментарного фактора питания, благотворно влияющего на организм и доступного для широких кругов населения.
Литература
- Riond J. L. Animal nutrition and acid-base balance // Eur J Nutr. 2001. № 40 (5). P. 245–254.
- Gannon R. H., Millward D. J., Brown J. E. et al. Estimates of daily net endogenous acid production in the elderly UK population: analysis of the National Diet and Nutrition Survey (NDNS) of British adults aged 65 years and over // Br J Nutr. 2008, Sep; 100 (3): 615–623.
- Adrogué H. E., Adrogué H. J. Acid-base physiology // Respir Care. 2001. Apr; 46 (4). Р. 328–341.
- Adrogué H. J., Madias N. E. Assessing Acid-Base Status: Physiologic Versus Physicochemical Approach // Kidney Dis. 2016. Nov; 68 (5). Р. 793–802.
- Todorovic J., Nešovic-Ostojic J., Milovanovic A.
 et al. The assessment of acid-base analysis: comparison of the «traditional» and the «modern» approaches // Med Glas (Zenica). 2015. Feb; 12 (1). Р. 7–18.
et al. The assessment of acid-base analysis: comparison of the «traditional» and the «modern» approaches // Med Glas (Zenica). 2015. Feb; 12 (1). Р. 7–18. - Prakova G. Monitoring of acid-base status of workers at a methyl methacrylate and polymethyl methacrylate production plant in Bulgaria // RAIHA J (Fairfax, Va). 2003. Jan-Feb; 64 (1). Р. 11–16.
- Manz F. History of nutrition and acid-base physiology // Eur J Nutr. 2001. Oct; 40 (5). P. 189–199.
- Greenhaff P. L., Gleeson M., Maughan R. J. The effects of dietary manipulation on blood acid-base status and the performance of high intensity exercise // Eur J Appl Physiol Occup Physiol. 1987. 56 (3). Р. 331–337.
- Greenhaff P. L., Gleeson M., Whiting P. H. et al. Dietary composition and acid-base status: limiting factors in the performance of maximal exercise in man? // Eur J Appl Physiol Occup Physiol. 1987. 56 (4). Р. 444–450.
- Remer T. Influence of nutrition on acid-base balance — metabolic aspects // Eur J Nutr. 2001. Oct; 40 (5). Р. 214–220.
- Remer T. Influence of diet on acid-base balance // Semin Dial. 2000, Jul-Aug; 13 (4): 221–226.
- Riond J. L. Animal nutrition and acid-base balance // Eur J Nutr. 2001 Oct; 40 (5): 245–254.
- Akter S., Eguchi M., Kurotani K. High dietary acid load is associated with increased prevalence of hypertension: the Furukawa Nutrition and Health Study // Nutrition. 2015 Feb; 31 (2): 298–303.
- СанПиН 2.1.4.10749–01 «Питьевая вода. Гигиенические требования к качеству воды».
- Malagelada J. R., Longstreth G. F., Summerskill W. H. et al. Measurement of Gastric Functions during Digestion of Ordinary Solid Meals in Man // Gastroenterology. 1976, 70 (2), 203–210.
- Hens B., Corsetti M., Brouwers J. et al. Gastrointestinal and Systemic Monitoring of Posaconazole in Humans After Fasted and Fed State Administration of a Solid Dispersion // J.
 Pharm. Sci. 2016, 105 (9), 2904–2912.
Pharm. Sci. 2016, 105 (9), 2904–2912. - Hunt J. N., Macdonald I. The Influence of Volume on Gastric Emptying // J. Physiol. 1954, 126 (3), 459–474.
- Rubbens J., Brouwers J., Wolfs K. et al. Ethanol Concentrations in the Human Gastrointestinal Tract after Intake of Alcoholic Beverages // Eur. J. Pharm. Sci. 2016, 86, 91–95.
- Feinle C., Kunz P., Boesiger P. et al. Scintigraphic Validation of a Magnetic Resonance Imaging Method to Study Gastric Emptying of a Solid Meal in Humans // Gut. 1999, 44 (1), 106–111.
- Coupe A. J., Davis S. S., Evans D. F. et al. Do Pellet Formulations Empty from the Stomach with Food? // Int. J. Pharm. 1993, 92 (1), 167–175.
- Heading R. C., Nimmo J., Prescott L. F. et al. The Dependence of Paracetamol Absorption on the Rate of Gastric Emptying // Br. J. Pharmacol. 1973, 47 (2), 415–421.
- Koziolek M., Grimm M., Garbacz G. et al. Intragastric Volume Changes after Intake of a High-Caloric, HighFat Standard Breakfast in Healthy Human Subjects Investigated by MRI // Mol. Pharmaceutics. 2014, 11 (5), 1632–1639.
- Mudie D. M., Murray K., Hoad, C. L. et al. Quantification of Gastrointestinal Liquid Volumes and Distribution Following a 240 mL Dose of Water in the Fasted State // Mol. Pharmaceutics. 2014, 11 (9), 3039–3047.
- Waldeyer H. W. Die Magenstraße. Sitzungsberichte der Koniglich — Preussischen Akademie der Wissenschaften; Verlag der Ko?niglich Preussischen Akademie der Wissenschaften: Berlin, 1908.
- Jefferson G. The Human Stomach and the Canalis Gastricus (Lewis) // J. Anat. Physiol. 1915, 49 (Part 2), 165–181.
- Baastrup C. I. Roentgenological Studies of the Inner Surface of the Stomach and of the Movements of the Gastic Contents // Acta Radiol. 1924, 3 (2–3), 180–204.
- Malagelada J. R., Go V. L., Summerskill W. H. Different gastric, pancreatic, and biliary responses to solid-liquid or homogenized meals // Dig.
 Dis. Sci. 1979, 24 (2), 101–110.
Dis. Sci. 1979, 24 (2), 101–110. - Malagelada J. R. Quantification of gastric solid-liquid discrimination during digestion of ordinary meals // Gastroenterology. 1977, 72 (6), 1264–1267.
- Pal A., Brasseur J. G., Abrahamsson B. A stomach road or «Magenstrasse» for gastric emptying // J. Biomech. 2007, 40 (6), 1202–1210.
- Ferrua M. J., Singh R. P. Computational modelling of gastric digestion: current challenges and future directions // Curr. Opin. Food Sci. 2015, 4, 116–123.
- Grimm M., Scholz E., Koziolek M. et al. Gastric Water Emptying under Fed State Clinical Trial Conditions Is as Fast as under Fasted Conditions // Mol Pharm. 2017, Dec 4; 14 (12): 4262–4271.
- Bateman D. N. Effects of meal temperature and volume on the emptying of liquid from the human stomach // J Physiol. 1982, Oct; 331: 461–467.
- Ritschel W. A., Erni W. The influence of temperature of ingested fluid on stomach emptying time // Int J Clin Pharmacol Biopharm. 1977 Apr; 15 (4): 172–175.
- Park E. J., Ryoo K. K., Lee Y. B. et al. Protective effect of electrolyzed reduced water on the paraquat-induced oxidative damage of human lymphocyte DNA // J. Korean Soc. Appl. Biol. Chem. 2005, 48, 155–160.
- Hanaoka K., Sun D., Lawrence R. et al. The mechanism of the enhanced antioxidant effects against superoxide anion radicals of reduced water produced by electrolysis // Biophys Chem. 2004, Jan 1; 107 (1): 71–82.
- Shirahata S., Kabayama S., Nakano M. et al. Electrolyzed-reduced water scavenges active oxygen species and protects DNA from oxidative damage // Biochem Biophys Res Commun. 1997, May 8; 234 (1): 269–274.
- Lee M. Y., Kim Y. K., Ryoo K. K. et al. Electrolyzed-reduced water protects against oxidative damage to DNA, RNA, and protein // Appl Biochem Biotechnol. 2006, Nov; 135 (2): 133–144.
- Yanagihara T., Arai K., Miyamae K. et al. Electrolyzed hydrogen-saturated water for drinking use elicits an antioxidative effect: a feeding test with rats // Biosci Biotechnol Biochem.
 2005, Oct; 69 (10): 1985–1987.
2005, Oct; 69 (10): 1985–1987. - Huang K. C., Lee K. T., Chien C. T. Reduced hemodialysis-induced oxidative stress in end-stage renal disease patients by electrolyzed reduced water // Kidney International. 2003, 64 (2), p. 704–714.
- Huang K. C., Yang C. C., Hsu S. P. et al. Electrolyzed-reduced water reduced hemodialysis-induced erythrocyte impairment in end-stage renal disease patients // Kidney Int. 2006, Jul; 70 (2): 391–398.
- Rubik B. Studies and observations on the health effects of drinking electrolyzed-reduced alkaline water // WIT Transactions on Ecology and The Environment. 2011. Vol. 153, 317–327.
- Landis G. N., Tower J. Superoxide dismutase evolution and life span regulation // Mech. Ageing Dev. 2005. Vol. 126, № 3. P. 365–379.
- Vorobjeva N. V. Selective stimulation of the growth of anaerobic microflora in the human intestinal tract by electrolyzed reducing water // Medical Hypotheses. 2005. 64 (3), p. 543–546,
- Wang Yu-Lian. Preliminary observation on changes of blood pressure, blood sugar and blood lipids after using alkaline ionized drinking water // Shanghai Journal of Preventive Medicin. 2001, 12.
- Jin D., Ryu S. H., Kim H. W. et al. Anti-diabetic effect of alkaline-reduced water on OLETF rats // Biosci Biotechnol Biochem. 2006, Jan; 70 (1): 31–37.
- Edy Siswantoro, Nasrul Hadi Purwanto, Sutomo Effectiveness of Alkali Water Consumption to Reduce Blood Sugar Levels in Diabetes Mellitus Type 2 // JDM. 2017, Nov, vol. 7, № 4, р. 249–264.
- Kim M. J., Kim H. K. Anti-diabetic effects of electrolyzed reduced water in streptozotocin-induced and genetic diabetic mice // Life Sci. 2006, Nov 10; 79 (24): 2288–2292.
- Kim M. J., Jung K. H., Uhm Y. K. et al. Preservative effect of electrolyzed reduced water on pancreatic beta-cell mass in diabetic db/db mice // Biol. Pharm. Bull. 2007, Feb; 30 (2): 234–236
- Li Y.
 , Nishimura T., Teruya K. et al. Protective mechanism of reduced water against alloxan-induced pancreatic beta-cell damage: Scavenging effect against reactive oxygen species // Cytotechnology. 2002, vol. 40, № 1–3, p. 139–149.
, Nishimura T., Teruya K. et al. Protective mechanism of reduced water against alloxan-induced pancreatic beta-cell damage: Scavenging effect against reactive oxygen species // Cytotechnology. 2002, vol. 40, № 1–3, p. 139–149. - Oostenbrug G. S., Mensink R. P., Hardeman M. R. et al. Exercise performance, red blood cell deformability, and lipid peroxidation: effects of fish oil and vitamin E // J Appl Physiol. 1997, Sep; 83 (3): 746–752.
- Paik I. Y., Jeong M. H., Jin H. E. et al. Fluid replacement following dehydration reduces oxidative stress during recovery // Biochem Biophys Res Commun. 2009; 383 (1): 103–107.
- Baskurt O. K., Meiselman H. J. Blood rheology and hemodynamics. Semin Thromb Hemost. 2003; 29 (5): 435–450.
- Halliwell B., Gutteridge J. Free radicals in medicine and biology. Oxford: Clarendon, 1999.
- Nwose E. U., Jelinek H. F., Richards R. S., Kerr P. G. Erythrocyte oxidative stress in clinical management of diabetes and its cardiovascular complications // Br J Biomed Sci. 2007; 64 (1): 35–43.
- https://www.lvrach.ru/2003/04/4530251/.
- Azizova O. A., Aseichev A. V., Piryazev A. P. et al. Effects of oxidized fibrinogen on the functions of blood cells, blood clotting, and rheology // Bull Exp Biol Med. 2007, Sep; 144 (3): 397–407.
- Weidman J., Holsworth R. E. Jr., Brossman B. et al. Effect of electrolyzed high-pH alkaline water on blood viscosity in healthy adults // J Int Soc Sports Nutr. 2016, Nov 28; 13: 45.
- Chycki J., Zajac T., Maszczyk A. et al. The effect of mineral-based alkaline water on hydration status and the metabolic response to short-term anaerobic exercise // Biol Sport. 2017, Sep; 34 (3): 255–261.
- Heil D., Seifert J. Influence of bottled water on rehydration following a dehydrating bout of cycling exercise // J Int Soc Sports Nutr. 2009; 6 (Suppl 1): 1–2.
- Chycki J., Kurylas A., Maszczyk A.
 et al. Alkaline water improves exercise-induced metabolic acidosis and enhances anaerobic exercise performance in combat sport athletes // PLoS One. 2018, Nov 19; 13 (11).
et al. Alkaline water improves exercise-induced metabolic acidosis and enhances anaerobic exercise performance in combat sport athletes // PLoS One. 2018, Nov 19; 13 (11).
Е. А. Хохлова, доктор медицинских наук
ООО «Медицинский центр «Август», Чебоксары
Контактная информация: [email protected]
DOI: 10.26295/OS.2019.16.75.011
Питьевая щелочная вода – насколько благотворно ее влияние на организм? Обзор литературы/ Е. А. Хохлова
Для цитирования: Лечащий врач № 6/2019; Номера страниц в выпуске: 44-49
Теги: физические нагрузки, кислотно-щелочной баланс, диабет
pH воды, воздействие на организм
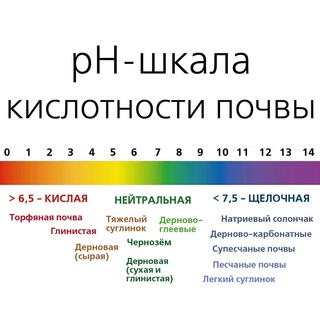
Potentia hydrogeni (pH) – водородный показатель. Он указывает на наличие в среде ионов водорода, количественно выражая кислотно-щелочной баланс питьевой воды. Показатель pH ниже 6,5-7 свидетельствует о повышенной кислотности среды. Если выше – это указывает на повышенную щелочность воды (концентрацию гидроксильных ионов).
Нормативные значения pH воды в Украине и ЕСВ Украине, кроме требований к очистке воды, также регламентируются и показатель pH воды. Он нормируется двумя стандартами:
- ГОСТ2874-82 – 6,0-9,0.
- ГСанПиН – 6,5-8,5.
Согласно европейскому стандарту качества, показатель кислотно-щелочного баланса питьевой воды в ЕС – 6,5-9,5.
Влияние кислотно-щелочного баланса воды на организм человекаОбщеизвестный факт, что для нормального функционирования организма человеку нужно употреблять в течение 1 дня от 1,5 до 2,5 литров чистой питьевой воды. Если фильтры для воды способны очистить среду от механических или бактериологических загрязнений, то для нормализации pH воды применяются природные кальциты и другие вещества.
Показатель кислотно-щелочного баланса спинномозговой, клеточной, межклеточной жидкости, лимфы, слюны и крови человека – 7,4-7,5.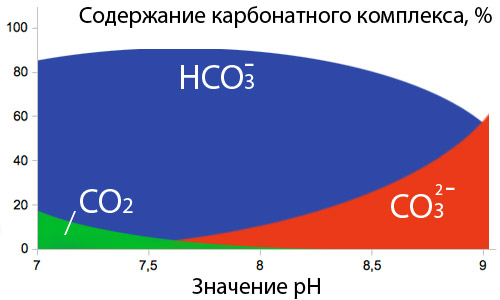 Если pH воды ниже, то она оказывает негативное воздействие на организм человека:
Если pH воды ниже, то она оказывает негативное воздействие на организм человека:
- нарушается обмен веществ;
- повышается риск отравлений;
- возникают проблемы с желудочно-кишечным трактом;
- сгущается лимфа, кровь, эритроциты, что препятствует обогащению клеток организма кислородом, выведению токсинов и приводит к образованию тромбов;
- кислая среда создает оптимальные условия для размножения и развития раковых клеток, гельминтов и вредных микроорганизмов, она разрушает клетки организма, что приводит к преждевременному старению;
- кислая вода не проникает в клетки, она скапливается и вызывает отеки;
- при низком уровне pH организму не хватает кремния и калия, магния и кальция, поэтому он «вытягивает» эти минералы из костных тканей, что приводит к остеопорозу;
- вода с низким показателем кислотно-щелочного баланса становится причиной стрессов, ухудшения сна, приводит к усталости и негативно влияет на состояние кожи.
Считается, что вода с повышенной щелочностью полезна для здоровья человека. Но это не так. Ученые доказали, что она негативно влияет на работу желудка и ухудшает ферментацию пепсина, который нейтрализует негативное воздействие бактерий на организм. Поэтому употребление воды с высоким показателем pH также вредно для здоровья людей.
Как можно нормализовать кислотно-щелочной баланс воды?Для определения уровня кислотно-щелочного баланса проводится бесплатный анализ воды.
Оптимальное оборудование для нормализации кислотно-щелочного баланса питьевой воды:
- Станции дозирования NaOH. Установки позволяют с помощью химических реагентов (амината БП, гидроксида натрия, гипохлорита натрия, коагулянтов, перманганата калия и др.) повышать уровень pH среды в линиях с постоянным или переменным расходом воды.
- Станции дозирования HCl – понижают кислотно-щелочной баланс питьевой воды путем дозирования различных реагентов: NaOCl (гипохлорита натрия), HCl (соляной кислоты), h3SO4 (серной кислоты), h3O2 (перекиси водорода), NaOH (едкого натрия) и KMnO4 (перманганата калия).

Для регулирования показателя pH в домашних условиях применяются фильтры для воды: для понижения кислотно-щелочного баланса – с мембранами обратного осмоса, для повышения – с картриджами-минерализаторами.
Проверка pH так же включается и в расширенный анализ воды позволяет подобрать наиболее эффективные методы и необходимые для повышения или понижения кислотно-щелочного баланса воды установки, реагенты, их количество и объем.
Общая щелочность как свойство воды
Щелочность воды — это способность раствора воды нейтрализовать сильную кислоту. Если в воду вносятся любые изменения, которые могут повысить или понизить значение рН, щелочность защищает воду и ее жизненные формы от резких изменений pH. Эта способность нейтрализовать кислоту или ионы Н+ особенно важна в регионах, пораженных кислотными дождями.
Теоретически, щелочность может быть вызвана любым слабым кислотным анионом, это, как правило, только угольная или бикарбонатная щелочность, которая важна для пресных вод. Щелочные вещества в воде включают гидроксиды или основания. Они могут быть обнаружены их острым вкусом соды.
Исследование по этому направлению:
Санитарно-химический анализ воды
На общую щелочность влияют факторы окружающей среды: дождь, дезинфицирующие вещества, добавление воды и др. Наибольшая щелочность в поверхностной воде происходит от карбоната кальция CaCO3, изымается из пород и почвы. Этот процесс усиливается, если горные породы и грунт разъединить по какой-либо причине, например, горнодобывающая промышленность или городское развитие. Известняк содержит особенно высокий уровень карбоната кальция, и при использовании для снижения кислотности в домах может происходить сток в поверхностные воды, может увеличить щелочность. Вода также может быть непригодной для использования в орошении, если уровень щелочности в воде превышает естественный уровень щелочности в почве.
В естественной среде угольная щелочность, как правило, составляет большую часть общей щелочности благодаря обычному возникновению и растворению карбонатных пород и наличии диоксида углерода в атмосфере. Другие общие природные компоненты, которые могут способствовать щелочности, включают борат, гидроксид, фосфат, силикат, нитрат, растворенный аммиак, коньюгатные основы некоторых органических кислот и сульфида.
Поскольку концентрация карбоната кальция увеличивается, щелочность также увеличивается, а риск подкисления уменьшается.
На самом деле можно регулировать уровень щелочности в организме сокращая пищевые продукты, которые производят кислоты, такие как кофеин, алкоголь, сода, мясо, молочные продукты, соль и сахар. Стоит только заменить эти продукты овощами и натуральными необработанными продуктами.
Другие материалы по этому направлению:
Можно ли пить воду с большим содержанием полифосфатов?
Можно ли пить воду с большим содержанием серебра?
Можно ли пить воду с большим содержанием нитратов?
Можно ли пить воду с большим содержанием магния?
Можно ли пить воду с большим содержанием никеля?
Можно ли пить воду с большим содержанием кальция?
Можно ли пить воду с большим содержанием цинка?
Можно ли пить воду с большим содержанием кобальта?
Можно ли пить воду с большим содержанием железа?
Опасность содержания хлора в питьевой воде
Можно ли пить воду, которая содержит нефтепродукты?
Безопасное содержание хрома в воде
Накопление алюминия в питьевой воде
Превышение нормы силикатов в воде
Формальдегид в питьевой воде
Озон при проведении дезинфекции воды
Бактерии E. coli в питьевой воде
Выявление энтеробактерий в питьевой воде
Гетеротрофные микроорганизмы в питьевой воде
Потребность в кремнии
Загрязнение воды колиформными бактериями
Влияние марганца на организм человека
Поверхностно-активные вещества
Без проведения анализа воды невозможно заметить щелочного состояния через бикарбонатные ионы, кроме случаев, когда они присутствуют в больших количествах. В отличие от этого, специалисты Судебной независимой экспертизы Украины легко обнаруживают щелочность через даже небольшое количество ионов карбоната и гидроксида.
В отличие от этого, специалисты Судебной независимой экспертизы Украины легко обнаруживают щелочность через даже небольшое количество ионов карбоната и гидроксида.
Высоко минерализованные щелочные воды вызывают чрезмерное высыхание кожи из-за того, что они склонны к удалению нормальных кожных масел.
Проблемные количества щелочности можно удалить обратным осмосом рядом с другими твердыми веществами. Другие способы очистки воды также удаляют общие растворенные твердые вещества, но они несколько менее подходят для домашнего использования по сравнению с обратным осмосом. Такими методами являются дистилляция и деионизация (деминерализация).
Популярные материалы:
Анализ воды — Зеленый корридор
Влияние высокого рН и щелочности на питание растений
В последнее время многие производители, которые используют полив, выразили беспокойство в связи с «высоким рН» их поливной воды и его неблагоприятного воздействия на растения.
Щелочность и рН являются двумя важными факторами при определении пригодности воды для полива растений. рН является мерой концентрации ионов водорода (Н+) в воде или другой жидкости. В целом, вода для орошения и точечного полива должна иметь рН в диапазоне от 5,0 до 7,0. Воду с рН ниже 7,0, называют «кислой», а воду с рН выше 7,0 — «основной»; рН 7,0 является «нейтральным». Иногда термин «щелочная» используется вместо «основной» и часто «щелочная» путают с «щелочностью». Щелочность является мерой способности воды нейтрализовать кислотность. Тест на щелочность измеряет уровень бикарбонатов, карбонатов и гидроксидов в воде и результаты испытаний, как правило, выражаются как «части на миллион карбоната кальция (CaCO3)». Желательный диапазон для поливной воды составляет от 0 до 100 частей на миллион карбоната кальция. Уровни от 30 до 60 частей на миллион считаются оптимальными для большинства растений.
Тесты оросительной воды всегда должны включать как рН так и щелочность. Испытание рН само по себе не является показателем щелочности. Вода с высокой щелочностью (т.е. высокий уровень бикарбонатов или карбонатов) всегда имеет значение рН ÷ 7 или выше, а вода с высоким рН не всегда обладает высокой щелочностью. Это важно, поскольку высокий показатель щелочности оказывает наиболее существенное влияние на питания растений.
Испытание рН само по себе не является показателем щелочности. Вода с высокой щелочностью (т.е. высокий уровень бикарбонатов или карбонатов) всегда имеет значение рН ÷ 7 или выше, а вода с высоким рН не всегда обладает высокой щелочностью. Это важно, поскольку высокий показатель щелочности оказывает наиболее существенное влияние на питания растений.
Влияние рН води на доступность элементов питания
Больше беспокойства вызывает тот случай, когда вода, имеющая высокий уровень рН и высокую щелочность используется для орошения. Одним из результатов этого является то, что рН среды выращивания может увеличиться со временем. Это увеличение может быть настолько большим, что нормальная доза извести должна быть уменьшена на целых 50%. В действительности вода действует как разбавленный раствор известняка. Проблема является наиболее серьезной, когда растения выращиваются в небольших контейнерах, поскольку малые объемы почвы плохо реагируют на изменение рН. Таким образом, сочетание высокого уровня рН и высокой щелочности вызывает особую озабоченность при выращивание рассады и растений в контейнерах. Недостатки кальция (Са) и магния (Mg) могу возникнуть в результате полива водой с высокой щёлочностью. Гораздо труднее прогнозировать влияние оросительных вод имеющей высокое значение рН и высокую щелочность на цветочные культуры открытой почвы, сады и ландшафтные растения. С одной стороны, долгосрочное орошение культур водой с высоким количеством гидрокарбонатов и карбонатов приводит к недостачи микроэлементов, которая может быть исправлена с помощью специальных удобрений.
помогает стабилизировать рН питательной среды возможно использовать для воды любого качества защищает систему полива от образования налёта солейС другой стороны при совокупности нескольких факторов, действующих вместе, возможно частично компенсировать последствия высокой щелочности воды. Во-первых, относительно высокое количество осадков вызывает вымывания ионов кальция и магния из почвы. Они заменяются на H +, и результатом является кислотность почвы. Во-вторых, кислотообразующими удобрениями, которые помогают противодействовать высоким рН и щелочности.
Они заменяются на H +, и результатом является кислотность почвы. Во-вторых, кислотообразующими удобрениями, которые помогают противодействовать высоким рН и щелочности.
А) Б)
Капельное орошение: а) культуры открытой почвы; б) горшечные растения
В дополнение к нарушению питания растений, вода с высокой щелочностью может вызвать другие проблемы. Бикарбонаты и карбонаты могут засорить форсунки распылителей пестицидов и труб систем капельного орошения с очевидными последствиями. Активность некоторых пестицидов, цветочных консервантов и регуляторов роста заметно снижается при высокой щелочности.
При смешивании с водой некоторые пестициды должны подкислить раствор, чтобы быть полностью эффективным. Могут потребоваться дополнительные подкислители, чтобы нейтрализовать всю щелочность. Для того, чтобы определить, является ли химическое вещество инициатором высокой щелочности, внимательно изучите этикетку продукта. К сожалению, это потенциально важная информация, которая не всегда печатается на этикетке, так что нужно приложить усилие, чтобы найти нужною информацию. Звонок к производителю, вероятно, будет необходим для большинства химических веществ. Многие тепличные операторы вводят кислоту (например, фосфорную, азотную или серную) в воду с проблемным высоким уровнем щелочности. Подкисление воды, имеющею высокую рН, но низкую щелочностью делают редко. Использование кислоты необходимо проводить очень осторожно по нескольким причинам:
— Во-первых, это дополнительный шаг в производстве, который потребует дополнительных материалов и оборудования.
— Во-вторых, кислоты опасны в обращении и может привести к повреждению некоторых форсунок и систем трубопроводов.
— В-третьих, фосфорная или азотная кислоты являются источниками Р и NO3, поэтому обычная программа внесения удобрений должна быть модифицирована с учесть добавленных питательных веществ.
Это будет зависеть от того, сколько кислоты необходимо использовать для нейтрализации щелочности и снижения рН. В-четвертых, иногда введение кислоты вызывает связывание элементов и перевод их в недоступную форму.
Количество кислоты, необходимое для достижения желаемого рН (т.е. нейтрализацию щелочности) определяют лабораторным титрованием пробы воды с соответствующей кислотой или с помощью расчета. Кислоту всегда вводят перед добавлением удобрений или других химических веществ.
Вода и кислотность кофе: как адаптировать состав воды к различным методам экстракции – 25 Magazine, Issue 9
Д-Р МАРКО УЭЛЛИНГЕР (MARCO WELLINGER) из Цюрихского университета прикладных наук (Zurich University of Applied Sciences, ZHAW), находящегося в г. Веденсвиль в Швейцарии, объясняет, почему щелочность важнее кислотности и почему нужно корректировать состав воды с учетом пропорций при приготовлении напитка и метода экстракции.
Даже когда на землю падают капли дождя, в них уже проникают газы, в основном CO2. Растворенный CO2, вступая в соединение с водой, образует угольную кислоту, поэтому кислотность дождевой воды всегда составляет около 5,5. По этой причине любая дождевая вода по определению является кислой средой. Однако следует отличать ее от такого явления, как обусловленный загрязнением воздуха оксидами серы и азота кислотный дождь, водородный показатель которого составляет 4,5 или менее. Такой дождь представляет угрозу для окружающей среды и зданий.
Начнем с вопроса о том, почему я пишу о дождевой воде и водородном показателе. Оказывается, кислотный дождь — идеальный пример для демонстрации возможностей щелочности по сравнению с водородным показателем. Один литр среднестатистической водопроводной воды в США с показателем щелочности 150 частей на миллион (чнм) CaCO3 может нейтрализовать 100 л дождя с водородным показателем 4,5.[1] Если применить ту же логику к воде и кофе, мы увидим, что щелочность влияет на окончательную кислотность напитка в несколько сотен раз сильнее, чем водородный показатель, при условии что водородный показатель близок к нейтральному значению (6—8), а щелочность достаточно высока (более 20 чнм CaCO3).
Водородный показатель и щелочность
О чем значение водородного показателя воды говорит вам как пользователю? Наиболее распространенное объяснение — «водородный показатель отражает кислотность воды» — в общих чертах верно, но не раскрывает тот важный факт, что измерение водородного показателя не дает представления об общем уровне кислотности. Оно лишь позволяет понять количество кислоты по отношению к нейтральному значению водородного показателя (см. стр. 21). Чтобы лучше проиллюстрировать этот принцип, я попрошу вас вспомнить соотношение между понятиями «температура» и «накапливаемое предметом тепло».
Возьмем, например, деревянную и каменную скамейки, стоящие вдоль одной дорожки в освещенном солнцем парке. Деревянная скамейка не будет очень горячей на ощупь, даже если солнце светит на нее весь день, каменная же, освещаемая тем же солнцем так же долго, напротив, будет невыносимо горячей. Измерения с помощью инфракрасного термометра, вероятно, покажут одинаковую температуру, но при этом в каменной скамейке, в основном из-за большой массы, будет много накопленного тепла, которое она передаст вам, если вы неосмотрительно решите присесть на нее.
Иллюстрация Эшли Элендер Стрэндкуист (Ashely Elander Strandquist).
Каменная скамейка — по той же причине — будет гораздо дольше сохранять тепло после захода солнца. Одним словом, в каменной скамейке будет больше накопленного тепла (она будет обладать большей теплоемкостью) при заданной температуре по сравнению с деревянной. Таким образом, каменная скамейка будет обладать более высоким сопротивлением к изменениям температуры, поскольку отличается высокой инерцией.
Давайте вернемся к воде. Водородный показатель отражает текущее состояние воды, но не содержит никакой информации о том, насколько легко он будет изменяться, когда в действие вступят кофе, газы или металлические нагревательные приборы. Как в случае с термометром и скамейками, водородный показатель не сообщит вам всех подробностей. В примере со скамейками было полезно узнать о теплоемкости, прежде чем решать, на какую из них сесть. При определении состава воды вам нужна дополнительная информация о щелочности. Она дает представление о сопротивляемости воды изменениям или отсутствии такого свойства. Таким образом, водородный показатель так же относится к щелочности, как температура к количеству накапливаемого тепла.
Низкий водородный показатель означает, что вода обладает кислой средой, но не говорит о количестве кислоты или, иными словами, о том, сколько кислоты потребовалось, чтобы снизить его до значения меньше 7. С точки зрения органолептических показателей именно это играет наибольшую роль: восприятие кислого вкуса напрямую связано с уровнем титруемой кислотности напитка. Фактически кислый вкус конкретного кофейного напитка соответствует количеству кислот, экстрагированных из кофе, с учетом уровня щелочности воды.
Что это означает для профессионалов в области кофе? Когда речь идет о выборе воды для экстракции кофе, гораздо более важно поддерживать определенный уровень щелочности, чем водородного показателя.
Адаптация состава воды к различным методам экстракции
Оказывается, правильное представление о щелочности и водородном показателе позволяет понять, как взаимодействуют кофе и вода, формируя кислотность напитка в вашей чашке. Важнейшей составляющей этого соотношения, помимо щелочности, являются пропорции при экстракции кофе. Диапазон методов экстракции кофе показывает десятикратную разницу в пропорциях (от 1,5 для ристретто до 15 для фильтрованного кофе). Это значит, что в наиболее концентрированных видах кофе (напитках типа эспрессо) используется только 10% воды для того же количества кофе, что в наиболее разбавленных напитках (фильтрованном кофе).
Это также значит, что для напитков типа эспрессо в вашем распоряжении есть только 10% щелочности, создающей буфер для присутствующих в кофе кислот, по сравнению с фильтрованным кофе с таким же количеством кислот. Из этого следует, что при заваривании эспрессо щелочность воды может быть гораздо выше, прежде чем она окажет значительное влияние на кислотность напитка. Ту же логику можно применить к общей жесткости, но разница состоит в том, что нет четкого ответа на вопрос о том, как именно общая жесткость влияет на экстракцию. Результаты наблюдений из различных источников показывают тенденцию к избыточному экстрагированию при высоком уровне общей жесткости (> 250 чнм CaCO3) и, наоборот, к недостаточному экстрагированию при низком уровне общей жесткости (< 40 чнм CaCO3), что отражается на вкусе. Тем не менее, экспериментальные измерения дают основания полагать, что влияние общей жесткости на общую эффективность экстрагирования незначительно при допустимых колебаниях уровня общей жесткости (20—250 чнм CaCO3).
Следование этой логике позволяет прийти к выводу, что существующие рекомендации относительно воды, основанные на приготовлении фильтрованного кофе или экспериментах в каппинге, необходимо изменять при приготовлении эспрессо в соответствии с применяемыми пропорциями. Однако такой подход приводит к техническим трудностям, с которыми мы сталкиваемся в реальности: подобное изменение состава воды приведет к значительному образованию накипи в кофемашине эспрессо.
Осложнения в реальном мире
Комитет стандартизации объединенной Ассоциации спешиэлти кофе (SCA) стремится разработать единый стандарт для воды, который сочетал бы старый стандарт Американской ассоциации (SCAA) и нормы основных регионов, относящихся к Европейской ассоциации (SCAE), и в то же время был усовершенствован с учетом вариантов пропорций заваривания для разных кофейных напитков, от эспрессо до фильтрованного. Этот стандарт все еще обсуждается, и приведенное исследование предлагает возможный подход к проблеме (рис. 1).
Fig. 1: Adopting water recommendations for espresso beverage ratios. Left: Simply scaling up the SCA standard would lead to heavy scale formation. Right: Safe zone for espresso machines and water boilers.Рис. 1. Принятие рекомендаций относительно воды для пропорций при приготовлении эспрессо. Слева: простое увеличение значений стандарта SCA приведет к образованию большого количества накипи. Справа: диапазон, безопасный для кофемашин эспрессо и приборов для нагревания воды.
Чтобы увеличить значения стандарта для приготовления эспрессо, стандартный показатель для фильтрованного кофе умножили на 7,3, что соответствует отношению между пропорциями для эспрессо (коэффициент пропорциональности = 2) и фильтрованного кофе (коэффициент пропорциональности = 14,6). Однако в таком случае новый стандарт для эспрессо будет находиться в пределах, предполагающих образование крайне большого количества накипи (0,25—0,45 г на каждый литр воды), что ограничит оптимальный диапазон, поскольку необходимо будет избегать составов воды, приводящих к образованию сильной накипи или ржавчины. Значения, которые останутся в «технически безопасных» границах, можно увидеть на рис. 1.
По сравнению со стандартом SCA для приготовления фильтрованного кофе это приведет к уменьшению рекомендуемой нижней границы общей жесткости (до значения 20 чнм CaCO3) и, в особенности, к гораздо большим показателям рекомендуемой щелочности — до 150 чнм CaCO3. Но помните, что нижняя граница общей жесткости установлена только по органолептическим, а не по техническим соображениям.
Таким образом, если вы заинтересованы в изучении составов воды для экстракции, то обнаружите, что новый стандарт очень ограничивает, но если вас интересуют эксперименты с более высокой щелочностью для смягчения кислого вкуса конкретного кофе, возможностей у вас больше. Если вы не хотите подбирать состав воды самостоятельно, добавляя к ней соли, в большинстве случаев лучше всего использовать смягчающий картридж (который только снижает общую жесткость), чтобы получить воду с высокой щелочностью, но низкой общей жесткостью, которая не будет приводить к образованию накипи в нагревательном приборе.
Д-Р МАРКО УЭЛЛИНГЕР занимается исследованиями кофе в области химии, технологий и органолептического анализа в Институте химии и биотехнологий Цюрихского университета прикладных наук в г. Веденсвиль.
[1] «Нейтрализация» воды означает повышение ее водородного показателя до 7. Вот как это возможно: дождевая вода обладает нулевой щелочностью, поэтому небольшое количество газов, образующих в воде кислоты, приводит к существенному снижению водородного показателя. При формировании кислотного дождя присутствуют газы CO2, NO2 и SO4. Они растворяются и образуют кислоты: угольную, азотную и серную соответственно.
В среднем водопроводная вода в США имеет щелочность 150 чнм CaCO3 и общую жесткость около 170 чнм CaCO3; таким образом, ее жесткость является средней. Даже в непроточном состоянии она представляет собой буферный раствор, в сотни раз более мощный, чем концентрация кислоты в кислотном дожде. Поэтому всего лишь один литр водопроводной воды может нейтрализовать сотни литров кислотного дождя.
Поговорим о воде: основные принципы
Пропорции напитка и пропорции заваривания
В настоящее время применяется несколько концепций, касающихся пропорций заваривания. Я предлагаю ввести термин «пропорции напитка», чтобы четко разделить два понятия.
Пропорции заваривания
- Применяются при стандартном приготовлении в пуровере или аэропрессе, где количество воды для заваривания (объем или вес) дается из расчета на вес молотого кофе
- Обычно записываются как отношение количества молотого кофе к объему воды (60 г на литр) или отношение веса воды к весу кофе (16,7, т. е. 1000 г воды, разделенные на 60 г кофе)
- Представляют собой удобные числовые показатели для приготовления напитка или адаптации рецептов к различным объемам
Пропорции напитка
- Используются в основном для эспрессо, формируются на основании веса напитка и веса молотого кофе
- Например, приготовление 36 г напитка из 18 г молотого кофе дает коэффициент пропорциональности, равный 2
- Позволяют ориентироваться на напиток, удобны для расчета процента экстракции
Водородный показатель
С научной точки зрения определение водородного показателя, или отрицательного логарифма концентрации ионов водорода, дает количественную оценку концентрации протонов (точнее, ионов водорода). Кроме того, он изменяется в логарифмическом масштабе, или по порядку величины, то есть уменьшение на одну единицу (-1) соответствует десятикратному увеличению концентрации протонов.
Карбонатная жесткость
Карбонатная жесткость представляет собой еще один способ выразить общий минимальный показатель общей жесткости и щелочности. Ее можно объяснить с помощью простой метафоры. Представьте себе партнеров по танцам. Количество пар, которое вы можете сформировать, ограничено численностью меньшей из двух групп: тех, кто хочет вести, и тех, кто хочет следовать за партнером. Таким образом, если вы хотите быть уверены, что в нагревательном приборе формируется защитный слой в размере не менее 40 мг на литр воды, ни общая жесткость, ни щелочность не могут быть ниже 40 мг CaCO3 на литр (40 чнм CaCO3).
Вы являетесь членом SCA? Получите бесплатную подписку на печатную версию журнала 25 Magazine на английском языке на странице sca.coffee/signmeup.
Не состоите в SCA? Вступайте уже сейчас и поддержите миссию нашей некоммерческой отраслевой ассоциации на sca.coffee/join.
Щелочность, кислотность или почему вода в бассейне зелёного цвета?
Отношение кислоты к щелочи в жидкости варьируется от 0 до 14. Средний уровень здесь равен 7 пунктам, что свидетельствует о нейтральном уровне жидкости. Если значение меньше 7, значит, в воде преобладает кислота, в противном случае больше щелочи. Впрочем, выдерживать строго этот коэффициент не стоит, колебания от среднего вполне возможны, скажем, если pH равен 3 или 4, данную воду вполне можно пить.Однако и пренебрегать соотношением кислоты и щелочи не следует, так как через какое-то время использования бассейна возможно придется менять трубы, насосы, фильтры и нагреватели, что может довольно сильно ударить по бюджету. Ошибочно полагают те, кто считают зеленый цвет воды результатом отсутствия в жидкости хлора, на самом деле это повышенный уровень pH.
Наилучшим значением коэффициента являются цифры в пределах от 7,2 до 7,4. Если соотношение меньше 7, вода в бассейне приобретает агрессивный характер и серьезно влияет на металлические детали, находящиеся в конструкции бассейна, вода быстро потребляет хлор. Если pH превышает восьмерку, хлор не так сильно дезинфицирует воду, что приводит, как уже было сказано, к появлению зеленого цвета. Это произойдет даже если увеличить дозу хлора на единицу объёма воды. Такая вода негативно влияет на кожный покров и глаза. И здесь проблема не в хлоре, а именно в соотношении кислоты и щелочи. Кроме того, повышенный уровень может привести к выходу из строя водонагревательных элементов, а также засорам.
Коэффициент pH рекомендуется проверять как минимум раз в неделю и поддерживать его на необходимом уровне. Для регулирования существуют специальные химические средства.
Общая щелочность — ТА
Общий уровень щелочности обычно путают со щелочностью. Первый параметр определяет число щелочных элементов в жидкости, рассчитывается в числе на миллион, либо в градусах.
Идеальное значение ТА — 100…150 ppm
При значении TA более 175 для регулирования соотношения кислоты и щелочи придется добавлять большее количество соответственно щелочи либо кислоты. Если TA ниже 60, уровень pH носит нестабильный характер, а, значит, его довольно трудно отрегулировать до необходимого значения, здесь понадобится достаточно терпения и выдержки.
Кальциевая жесткость — СН
Жесткость по кальцию характеризует, какое число частиц, содержащих кальций, растворяется в жидкости. Т.к. кальций растворяется хуже других находящихся в воде элементов, этот параметр является очень важным. Здесь мы расскажем о том, как правильно выбирать химикаты для добавления в воду бассейна, при этом необходимо руководствоваться жесткостью воды. При высоком уровне кальций будет осаждаться на оборудовании бассейна, что сделает воду мутной. Это будет более заметным при высоком соотношении кислоты и щелочи. Для смягчения необходимо добавить более мягкой воды, а при низком уровне жесткости следует пользоваться соединениями хлора и кальция.
Загрязнение водыЩелочность воды — это показатель того, сколько кислоты она может нейтрализовать. Если в воду вносятся какие-либо изменения, которые могут повысить или понизить значение pH, щелочность действует как буфер, защищая воду и ее жизненные формы от внезапных изменений значения pH. Эта способность нейтрализовать кислоту или ионы H + особенно важна в регионах, пострадавших от кислотных дождей. Что влияет на щелочность? Общая щелочность зависит от факторов окружающей среды; дождь, кислотные дезинфицирующие средства, добавление воды для наполнения и другие применения продукта могут со временем изменить щелочность. Наибольшая щелочность поверхностных вод происходит из-за выщелачивания карбоната кальция CaCO3 из горных пород и почвы. Этот процесс ускоряется, если камни и почва были расколоты по какой-либо причине, например, в результате горных работ или городского строительства. Известняк содержит особенно высокий уровень карбоната кальция, и когда его используют для снижения кислотности в домах, он может стекать в поверхностные воды и повышать щелочность.Щелочность имеет большое значение при очистке сточных вод и питьевой воды, поскольку она влияет на процессы очистки, такие как анаэробное сбраживание. Вода также может быть непригодной для использования при орошении, если уровень щелочности воды выше естественного уровня щелочности почвы.
Щелочность также тесно связана с кислотонейтрализующей способностью (ANC) раствора, и ANC часто неправильно используется для обозначения щелочности.Тем не менее, способность нейтрализовать кислоту относится к комбинации присутствующего раствора и твердых веществ (например, взвешенных веществ или твердых частиц водоносного горизонта), и доля твердых веществ может преобладать над ANC (см. Карбонатные минералы выше).
|
Какая щелочность в питьевом вате
Щелочность означает способность воды нейтрализовать кислоты.Он может измерять присутствие бикарбоната, диоксида углерода, ионов гидроксида и карбоната, которые естественным образом присутствуют в воде.
Уровень pH питьевой воды означает, насколько она щелочная или кислая. Уровень pH относится к ионам водорода, содержащимся в воде. Это означает «потенциал водорода». Уровень pH воды при нормальном питьевом уровне, карбонаты и бикарбонаты являются основными факторами, влияющими на ее щелочность.
Что такое щелочность питьевой воды?Щелочность — это способность воды противостоять изменениям pH, которые делают воду более кислой.Когда дело доходит до питьевой воды, он также помогает защитить ваше здоровье и трубопроводы.
Термин «буферная емкость» обычно обозначает эту емкость. Щелочность также относится к способности воды нейтрализовать кислоту. На самом деле это правда, что он имеет буферную емкость. Буфер — это раствор, в который можно добавлять кислоту без изменения концентрации доступных ионов H + (как при изменении pH). Он поглощает избыточные ионы H + и защищает воду от колебаний pH.
Например, если вы добавите один и тот же раствор слабой кислоты в два флакона с водой — оба с pH 7.Один — с нулевой щелочностью или буферной способностью. Другой имеет буферную способность (например, щелочность 50 мг / л) — pH воды с нулевой щелочностью немедленно упадет, в то время как pH забуференной воды изменится с очень небольшого до нулевого. pH буферного раствора изменится, когда буферная емкость раствора будет перегружена.
Что меняет щелочность?На pH и уровень щелочности колодезной воды могут влиять различные факторы, такие как кислотные дезинфицирующие средства, дождь, добавление воды для наполнения, а также другие применения продуктов, которые могут изменять уровень щелочности с течением времени.Большая часть щелочности поверхностных вод обусловлена карбонатом кальция CaCo3, который выщелачивается из почвы и горных пород.
Этот процесс ускоряется, если почва и горные породы были раздроблены по разным причинам, например, в результате городского строительства или горнодобывающей промышленности. Известняк содержит большое количество карбоната кальция. Когда он используется для снижения кислотности в домах, он может стекать в поверхностные воды и повышать уровень щелочности.
Щелочность важна при очистке сточных вод и питьевой воды.Это может повлиять на процессы лечения, такие как анаэробное пищеварение. Вода также может стать непригодной для орошения, если ее щелочность превышает естественный уровень щелочности почвы.
| US EPA Категория | Концентрация карбоната кальция (мг / л) |
| Подкисленный | <1 |
| Критическое | <2 |
| Находящиеся под угрозой исчезновения | 2-5 |
| Высокочувствительный | 10-20 |
| Не чувствительно | > 20 |
Щелочность тесно связана с кислотонейтрализующей способностью (ANC) раствора.Часто АНК неправильно используется для обозначения щелочности. Но способность нейтрализовать кислоту может относиться к комбинации доступного раствора и твердых веществ. Примерами являются твердые частицы водоносного горизонта и взвешенные вещества.
Как измерить щелочностьИзмерение щелочности
Титрование — это процесс измерения щелочности. «Титрант» представляет собой кислоту известной силы, которую добавляют в объем обработанной пробы воды. Объем кислоты, необходимый для доведения образцов до определенного уровня pH, отражает щелочность образца.Изменение цвета указывает на конечную точку pH. Единица измерения щелочности — миллиграммы на литр (мг / л) CaCO3 (карбоната кальция).
Измерение щелочности
Геологическая служба США (USGS) использует один общий метод измерения щелочности. Необходимо взять образец воды и добавить к нему кислоту, а затем проверить pH воды по мере добавления кислоты. Он снимает начальные показания воды и добавляет небольшое количество кислоты, перемешивает, а затем измеряет ее pH. Одни и те же шаги повторяются много раз.
Во-первых, соединения в воде, такие как бикарбонаты, нейтрализуют добавляемые кислоты. Чем больше добавляется кислоты, тем бикарбонаты «расходуются», поскольку они нейтрализуются кислотой. До тех пор, пока в конце концов не будут израсходованы все нейтрализующие кислоту соединения. После этого кислота в воде будет линейно понижать pH. Ученый сможет увидеть эту точку отражения, просмотрев линейную диаграмму количества кислоты, добавленной в воду, и результирующего pH. Точка, в которой изменение линии pH становится линейным, определяет щелочность воды.
На этом снимке ученый Геологической службы США выполняет титрование щелочности, чтобы определить щелочность пробы воды. Обратите внимание на рН-метр на заднем плане, показывающий на данный момент 5,477. Зонд pH — это большая серая трубка, входящая в стакан. Черное устройство с правой стороны проталкивает фиксированное количество кислоты через белую трубку, которая идет в правую сторону стакана с водой. Черный ящик на дне имеет вращающийся магнит, который затем вращает небольшой магнит, расположенный на дне стакана, который поддерживает перемешивание пробы воды.
Факторы, влияющие на щелочность Геология и почвыВодная система накапливает карбонаты, если вода проходит через почву и породу, содержащую карбонатные минералы, такие как кальцит (CaCO3). Воды с известняком и осадочными породами и почвы, богатые карбонатами, имеют высокую щелочность. Восточная часть водораздела Боулдер-Крик является одним из примеров. Воды с вулканическими породами (такими как гранит) и твердыми частицами с низким содержанием карбонатов имеют низкую щелочность. Одним из примеров является западная часть водораздела Боулдер-Крик.
Изменение pHПоскольку pH и щелочность тесно связаны, изменения pH также могут влиять на щелочность. Это особенно актуально для потока с плохой буферизацией.
Отвод сточных водСточные воды очистных сооружений (очистных сооружений) могут повысить щелочность потока. Сточные воды из наших домов также содержат бикарбонат и карбонат чистящих средств и остатков пищи, которые мы сбрасываем в канализацию.
Степень и уровни щелочностиЩелочность при pH выше 8.3 в основном находится в форме карбоната (CO32-). С другой стороны, щелочность с pH ниже 8,3 присутствует в основном в виде бикарбоната (HCO3-).
Поскольку щелочность варьируется из-за различий в геологии, не существует установленных стандартов щелочности. Пресная вода обычно имеет уровень щелочности 20-200 мг / л. Общий уровень щелочности 100-200 мг / л может стабилизировать уровень pH в потоке. Уровни ниже 10 мг / л показывают, что вода плохо забуферена и очень чувствительна к изменениям pH из естественных и антропогенных источников.
Почему важна щелочность К водоемуЩелочность ближайшего водоема важна для здоровья и благополучия, например, озера. Экосистема и живущие в озере организмы адаптировались в водоемах, которые не претерпели быстрых изменений. До прибытия людей эти водоемы не подвергались кислотным дождям или разливам химических веществ. С рыбой в озере было все в порядке, пока pH и водные характеристики озера сильно не изменились за короткий период времени.
По сей день водные объекты уязвимы для внезапного попадания химикатов, например, содержащихся в кислотных дождях и сточных водах. Это может вызвать быстрые изменения кислотно-щелочного баланса озера — например, снижение pH воды в озере.
К водным организмам
Для рыб и других водных организмов необходим диапазон pH от 6,0 до 9,0. SInce защищает от быстрых изменений pH, щелочность помогает защитить живые организмы, которым необходим определенный диапазон pH. Более высокие уровни щелочности в поверхностных водах могут служить буфером для кислотных дождей и других кислотных отходов.Это может предотвратить опасные для водных организмов изменения pH.
К источнику питьевой воды
Щелочность также важна при рассмотрении вопроса об очистке питьевой воды и сточных вод, поскольку она влияет на процессы очистки, такие как анаэробное сбраживание. Когда уровень щелочности воды выше естественного уровня щелочности почвы, вода может быть непригодной для использования при орошении.
Уровень pH питьевой воды
Уровень pH воды измеряется по шкале от 0 до 14.Если результат измерения ниже 7, это означает, что вода кислая. Если он больше 7, значит вода щелочная или щелочная. Если 7, значит вода нейтральная.
Если уровень pH воды ниже 6,5, это может способствовать коррозии арматуры и труб. Кроме того, степень коррозии воды зависит от других факторов. Примерами являются общее количество растворенных твердых веществ, температура воды, щелочность и ее жесткость.
Кроме того, вода с балансом pH 6.5 не представляет опасности для здоровья. Но агрессивная вода способна растворять металлы, такие как цинк, кадмий, свинец и медь, которые содержатся в трубах. Таким образом, это может вызвать повышенную концентрацию металлов в питьевой воде. В долгосрочной перспективе это может привести к проблемам со здоровьем.
Между тем, если уровень pH выше 8,5, это может способствовать образованию накипи, особенно в водопроводе.
Уровень щелочности воды
Щелочность состоит из гидроксидов, бикарбонатов и карбонатов, которые объединяют магний, кальций и щелочь.Это компоненты, которые вы можете найти в антацидах, таких как Rolaids или Tums, щелок, пищевая сода и известняк. Если уровень щелочности высокий, потребуется больше кислоты, чтобы снизить уровень pH воды. Один из способов представить себе щелочность — это способность воды нейтрализовать кислоту.
Щелочность выражается в миллионных долях эквивалента карбоната кальция. Чем выше число, тем больше этих компонентов содержится в воде.
Вода с высокой щелочностью может привести к постепенному увеличению pH среды для выращивания.Когда уровень pH повышается, это отрицательно сказывается на доступности различных питательных веществ для растений, особенно таких микроэлементов, как марганец и железо. Теперь это может привести к дефектам.
Теперь может потребоваться добавить в воду минеральные кислоты, такие как фосфорная или серная кислота. Или используйте кислотные добавки, такие как кислотообразующие или сернистые минералы.
С другой стороны, в воде с низкой щелочностью отсутствуют компоненты, нейтрализующие кислоту. Продолжение использования кислых смесей может привести к нежелательному снижению уровня pH среды для выращивания.
В воде часто не хватает магния, кальция, сульфата или других добавок, которые могут потребоваться.
Тестирование скважинной воды на щелочность
Обязательным условием является регулярное тестирование воды из колодца на стандартные химические параметры, включая щелочность и уровень pH. Выберите для этого аккредитованную лабораторию по тестированию воды. Вы можете получить специальные бутыли для проб и инструкции в выбранной вами лаборатории.Стоимость анализа проб воды может варьироваться. Цена может варьироваться в зависимости от протестированных параметров и лаборатории.
При тестировании на щелочность сначала необходимо заполнить фильтрующую трубку водой до отметки 5 мл. Затем опустите в воду красную таблетку. Закройте его и встряхивайте, пока таблетка не исчезнет. Тогда вода может стать сине-зеленой. Если вода станет розовой, значит, она не содержит щелочности.
После этого заполните титрование с прямым считыванием реагентом для титрования щелочности B.Затем вы должны заполнить титр каждый раз, когда поршень достигает нулевой отметки. Когда поршень достигнет нулевой отметки, поместите титр, найденный в центральное отверстие колпачка титровальной трубки.
Медленно нажимайте на поршень, пока сине-зеленый цвет образца титрования не изменится на розовый. Количество Реагента B, которое снижается при титровании, когда он становится розовым, является доступным щелочным уровнем воды. Вы можете измерить его в частях на миллион (ppm) из 200 ppm.
Другой термин для определения щелочностиДругая терминология для щелочности — , жесткость воды . Таким образом, будет справедливо сказать, что щелочность и жесткость воды одинаковы, оба они происходят из природных источников. Когда вода движется сквозь камни, она собирает минералы по пути к рекам и озерам. Когда известняк и доломит растворяются в воде, одна половина молекулы — это кальций или магний («жесткость»), а другая половина — карбонат («щелочность»). Это означает, что уровень жесткости и щелочности воды в каком-либо месте будет очень похож.Но их измерения очень разные и имеют разное значение.
Действительно ли щелочная вода работает?
Использование щелочной питьевой воды вызывает споры. Некоторые эксперты в области здравоохранения утверждают, что недостаточно исследований, чтобы подтвердить заявления о пользе для здоровья, представленные продавцами и пользователями. Между тем, есть различия в результатах исследований, которые могут быть связаны с типом исследований щелочной воды.
По мнению экспертов, обычная вода по-прежнему остается лучшей для людей.Нет исследований, полностью подтверждающих утверждения сторонников щелочной воды.
Но есть некоторые исследования, которые показывают, что щелочная вода может быть полезна при определенных заболеваниях. Например, в исследовании, проведенном в 2012 году, было обнаружено, что употребление естественно газированной щелочной воды из артезианских колодцев с уровнем pH 8,8 может помочь дезактивировать пепсин. Это основной фермент, вызывающий кислотный рефлюкс.
Кроме того, употребление щелочной ионизированной воды может иметь положительные последствия для организма, особенно для людей с высоким кровяным давлением, высоким уровнем холестерина и диабетом.
В ходе исследования, проведенного несколько лет назад с участием около 100 человек, было обнаружено, что существует значительная разница в вязкости крови после приема воды с высоким pH. Это по сравнению с теми, кто употребляет обычную воду после тяжелой тренировки. Вязкость относится к прямому измерению кровотока по сосудам.
Те, кто пьет воду с высоким уровнем pH, могут иметь пониженную вязкость на 6,3% по сравнению с теми, кто пьет стандартную воду с вязкостью 3,36%. Таким образом, вы можете улучшить кровоток с помощью щелочной воды.Благодаря этому доставка кислорода в организм может быть увеличена.
Но для подтверждения этих исследований необходимы дополнительные исследования. Эта область нуждается в дополнительных исследованиях, чтобы дать ответы на другие утверждения, сделанные теми, кто поддерживает употребление щелочи.
Хотя научных исследований недостаточно, сторонники щелочной воды считают, что она приносит различную пользу для здоровья. В него входят:
- Антивозрастные свойства (благодаря жидким антиоксидантам, которые быстрее усваиваются в организме человека)
- Очищает толстую кишку
- Поддерживает иммунную систему
- Похудеть
- Увлажняет кожу и выводит из нее токсины
- Обеспечивает устойчивость к раку
Сторонники также утверждают, что кислые газированные напитки имеют положительный ОВП, что вызывает множество проблем со здоровьем.Между тем, подщелачиваемая и должным образом ионизированная вода имеет отрицательный ОВП. Зеленый чай обладает антиоксидантными свойствами и имеет небольшой отрицательный ОВП.
Щелочная вода и ее возможное лечение рака
Использование щелочной воды может помочь нейтрализовать кислоту, которая содержится в кровотоке тела. Считается, что питьевая вода с высоким уровнем pH может ускорить обмен веществ и улучшить способность организма усваивать необходимые питательные вещества.
Есть и другие теории, которые объясняют, что щелочная вода будет голодать раковые клетки в организме.Это потому, что раковые клетки стремятся в кислой среде. Больше щелочи в организме может остановить или замедлить рост раковых клеток, уравновешивая уровень pH в организме.
Таким образом, щелочная вода может оказывать увлажняющее действие на организм. По мнению других, это может даже улучшить симптомы некоторых заболеваний, таких как кислотный рефлюкс.
Но в организме с обычным функционированием щелочная вода, доступная в коммерческих магазинах, вообще не вызывает значительных изменений.Это не вызовет значительного изменения общего кислотно-щелочного баланса в кровотоке.
Как использовать щелочную воду
В 2011 году Всемирная организация здравоохранения (ВОЗ) выпустила обновленное руководство по качеству питьевой воды. Как правило, организация не дает никаких рекомендаций или указаний, касающихся здоровья, в отношении конкретного уровня pH питьевой воды.
В директивах указано, что уровень pH питьевой воды не оказывает прямого воздействия на потребителей.Это верно, поскольку вода, дезинфицированная хлором, имеет уровень pH менее 8,0.
Если вы хотите использовать щелочную воду, вы должны пить ее так же, как и водопроводную воду. Но имейте в виду, что употребление слишком большого количества щелочной воды может привести к возможным побочным эффектам, таким как несварение желудка или расстройство желудка.
Риски и возможные побочные эффекты питьевой щелочной воды
В общем, питьевая щелочная вода безопасна. Однако он все же может вызывать побочные эффекты на человеческий организм.Некоторые из побочных эффектов могут включать снижение уровня кислотности желудка. Это может помочь убить бактерии в организме. Он может изгнать нежелательные патогены в кровоток.
Кроме того, чрезмерная щелочность человеческого тела может вызвать раздражение кожи. Это также может привести к проблемам с желудочно-кишечным трактом. Кроме того, он может нарушить нормальный уровень pH в организме. Это может привести к метаболическому алкалозу — состоянию здоровья, которое может вызывать такие симптомы, как рвота, тошнота, подергивание мышц, тремор рук, спутанность сознания и покалывание в лице.
Метаболический алкалоз может привести к снижению уровня кальция в организме. Таким образом, это может нанести вред здоровью костей. Но самая частая причина гипокальциемии — не употребление щелочной воды. У него недостаточно активная паращитовидная железа.
Натуральный или искусственный?
Естественная щелочь возникает, когда вода проходит по камням, как в источниках. Затем он собирает минералы по пути, что вызывает повышение щелочного уровня.
Но современные дома, потребляющие щелочную воду, покупают продукт, химически обработанный посредством электролиза.
В этом методе используется продукт, который называется ионизатором. Он может повысить уровень pH обычной воды. Те, кто делает ионизаторы, утверждают, что электричество может разделять молекулы в воде, которая является более кислой и щелочной. После этого кислая вода удаляется.
Однако специалисты утверждают, что эти утверждения не подтверждаются достойными исследованиями.Качество воды исходного источника до начала ионизации важно для обеспечения того, чтобы загрязняющие вещества не попадали в питьевую воду.
С другой стороны, есть и другие ученые, предлагающие использовать обратный осмос. Благодаря этому он может надлежащим образом очищать воду перед подключением к щелочному ионизатору. Таким образом, он может добавлять минералы и повышать уровень pH воды.
Исследование, проведенное Всемирной организацией здравоохранения (ВОЗ), ограничивает использование питьевой воды с низким содержанием минералов.Это можно сделать с помощью дистилляции, обратного осмоса и других методов.
Где взять щелочную воду?
Щелочную воду можно купить в магазинах здоровой пищи или продуктовых магазинах. Вы также можете купить его в Интернете. Вы также можете пить газированную воду с высоким уровнем pH и естественной минерализацией.
Между тем ионизаторы воды продаются в различных крупных сетевых магазинах по всему миру.
С другой стороны, вы также можете самостоятельно приготовить щелочную воду в своем доме.Соки лайма и лимона обладают естественной кислотностью. Однако в них есть минералы, которые могут изменять состав воды. Просто добавьте в воду немного лайма или лимона, и теперь вы можете сделать ее более щелочной. Кроме того, вы можете добавить в воду капли пищевой соды, чтобы изменить ее уровень pH.
Если вы фильтруете воду, чтобы удалить загрязнения, повторно минерализовать или ионизировать ее, то нет никаких доказательств ограничения того, сколько щелочной воды вы можете потреблять ежедневно.
Безопасность щелочной воды
Многие эксперты в области здравоохранения не озабочены безопасностью щелочной воды.Но это больше касается заявлений о здоровье, которые они сделали по этому поводу.
Недостаточно научных данных, подтверждающих использование щелочной воды для лечения различных заболеваний. Фактически, несколько медицинских экспертов сделали предупреждение о его использовании из-за требований нескольких маркетологов.
Это правда, что питьевая щелочная вода в целом безопасна, поскольку она содержит различные природные минералы. Однако следует с осторожностью относиться к использованию искусственной щелочной воды. Это потому, что он содержит меньше минералов, чем необходимо организму.Возможно, это может содержать загрязняющие вещества, чем вы думали. В целом, его чрезмерное употребление может привести к дефициту минералов в организме.
Заключение
В целом, питьевая щелочная вода в целом безопасна для организма. Это приносит пользу своим потребителям, однако заявления не были подтверждены исследованиями качества. Есть еще кое-что, что необходимо проверить с его использованием, и потребуется больше лет, чтобы изучить его потенциал для здоровья человека.
Но если вы хотите пить щелочную воду, вы можете произвести ее самостоятельно, используя несколько фильтров, имеющихся на рынке. Вы также можете воспользоваться услугами надежных магазинов воды в вашем районе.
Похожие сообщения
- Что такое солнечная ферма? Каковы плюсы и минусы?
Знаете ли вы, что энергия, которую Солнце дает Земле в течение одного часа, может удовлетворить мировые потребности в энергии в течение одного года? Потребители и политики получают два варианта…
- Опасности, связанные с загрязнением в нерегулируемых частных колодцах
В среднем около 13 миллионов американских семей владеют частными колодцами. На частные колодцы не распространяется действие федерального законодательства, применимого к коммунальным системам питьевой воды …
- Лучшие методы экономии воды для домовладельцев
Общая емкость воды в мире постоянна. Ничего не приобретено и не потеряно. Вода испытывает постоянный гидрологический цикл осадков, инфильтрации, стока и EVA…
- Как Луна вызывает приливы на Земле?
«Приливы» — это общий термин, используемый для характеристики смены подъема и спада уровня океана по отношению к суше, создаваемого гравитационным притяжением Луны и Солнца ….
- Кофе хорош или вреден для вас?
Это неудивительно, ведь кофе — топливо для многих людей во всем мире. Считается самым любимым напитком. Так что велики шансы, что вы один из тех, кто…
- Водное правосудие во время COVID-19
По мере того, как COVID-19 продолжает свое разрушительное распространение, американцы моют руки чаще, чем когда-либо прежде. Большинство не особо задумываются о …
- Может ли вода помочь вам жить дольше? Секреты воды и долголетия.
Как долго вы ожидаете, что будете жить на Земле? Это непросто представить, но на самом деле люди живут дольше в 21 веке….
- Циклические проблемы утилизации ПФАС
В настоящее время существует 3 основных способа утилизации перфторалкильных и полифторалкильных веществ (ПФАС), опасных химикатов, используемых для изготовления противопожарной пены, и …
Щелочность воды в зависимости от pH в вашей питательной среде — в чем разница?
Назад
Четверг, 7 января 2021 г. | Трой Бюшель
Щелочность воды и pH не одно и то же.PH воды измеряет количество водорода (кислотных ионов) в воде, тогда как щелочность воды является мерой уровней карбонатов и бикарбонатов в воде. Думайте о карбонатах и бикарбонатах как о растворенном известняке. Чем выше щелочность воды, тем больше в ней извести и, следовательно, тем быстрее вода может вызвать повышение pH среды выращивания. С другой стороны, pH воды не влияет на pH питательной среды.
| pH исходной воды | Щелочность воды (ppm CaCO 3 ) | Серная кислота, необходимая для снижения pH воды до 5.0 (мл) |
| 9,3 | 71 | 1,2 |
| 8,3 | 310 | 6.0 |
Например, приведенная выше диаграмма показывает начальный pH двух источников воды и количество кислоты, необходимое для каждого из них, чтобы достичь pH 5,0. Вода с более высоким pH не требовала такого количества кислоты, как вода с более низким начальным pH. На первый взгляд, это может не иметь смысла. Однако обратите внимание на щелочность в центральной колонке.Независимо от исходного pH, чем выше щелочность источника воды, тем больше кислоты требуется для снижения pH до 5,0. Для всех источников воды именно щелочность определяет, сколько кислоты следует использовать, а не pH.
Как щелочность воды влияет на pH среды выращивания?
На приведенном ниже графике вилки барвинка выращивали в течение 49 дней и постоянно подкармливали одним и тем же удобрением в концентрации 125 частей на миллион. Пробки орошались тремя разными источниками воды с разной щелочностью.Уровень pH повысился во всех трех образцах среды частично из-за использованных удобрений и известняка в среде выращивания. Однако чем выше щелочность источника воды, тем выше pH среды для выращивания.
На этом графике показано влияние щелочности воды на pH пробок барвинка через 49 дней. Обратите внимание, чем выше щелочность воды, тем выше pH питательной среды через 49 дней. Данные взяты из: D. Bailey & P.V. Nelson, pH субстрата и качество воды.1996 Краткий курс Огайо
Понятно, что pH воды и щелочность не одно и то же. Фактически, pH воды не определяет pH среды для выращивания, но на самом деле именно щелочность источника воды влияет на pH среды для выращивания. Это важно для производителей, так как щелочность оказывает значительное влияние на pH среды выращивания при выборе правильного (ых) удобрения (й) и / или введения кислоты.
Для получения дополнительной информации свяжитесь с вашим представителем Premier Tech Grower Services:
Эд Бладник | Джоанн Пири | Лэнс Лоусон |
Трой Бюхель | Susan Parent | Хосе Чен Лопес |
PRO-MIX® — зарегистрированная торговая марка PREMIER HORTICULTURE Ltd.
Щелочность — обзор | Темы ScienceDirect
14.3.1.5 Риск низкой буферной емкости
Щелочность — это стандартизированная мера буферной емкости воды, то есть количественная способность оснований в воде нейтрализовать кислоты. Воды с низкой щелочностью очень чувствительны к изменению pH; по мере увеличения щелочности способность воды противостоять изменениям pH возрастает, увеличивая ее буферную способность. Буферными основаниями в первую очередь являются бикарбонат (HCO 3 — ) и карбонат (CO 3 2 — ), а щелочность обычно выражается как эквивалентная концентрация карбоната кальция (CaCO 3 ).Щелочность также напрямую связана с жесткостью воды, которая определяется концентрацией многовалентных катионов (в первую очередь Ca 2 + и Mg 2 + ) в воде. CCPP — это практический параметр, который прогнозирует количество карбоната кальция, которое может выпадать в осадок в данной воде.
Пермеат обратного осмоса характеризуется очень низким pH, щелочностью и жесткостью воды, поскольку мембраны очень эффективно удаляют бикарбонаты и карбонаты. Эти характеристики делают пермеат обратного осмоса агрессивным даже по отношению к компонентам распределительной системы [29].Чтобы избежать возможных проблем, связанных с химической нестабильностью в ТБО по схемам распределения, щелочность и жесткость воды должны достигаться с помощью процессов доочистки на SWDP [30]. Если ГСВ поставляются для орошения сельскохозяйственных культур, высокие значения щелочности рекомендуются по ряду причин: для минимизации коррозии в распределительных системах, где очень часто встречаются металлические элементы, такие как рабочие клапаны и устройства; свести к минимуму выброс ионов металлов в воду, чтобы предотвратить ржавление труб, приводящее к более высоким потерям напора в металлических трубах; и для стабилизации pH при добавлении кислых или основных удобрений в масштабе фермы [20].
Фертигация и беспочвенные культуры являются распространенной практикой в высокотехнологичном сельском хозяйстве, где поток ТБО обычно зависит от добавления удобрений, а внезапные изменения рН ТБО могут иметь сильное влияние на доступность питательных веществ для сельскохозяйственных культур и, в конечном итоге, на продуктивность сельского хозяйства. Тогда достаточная буферная емкость ТБО особенно актуальна для сельского хозяйства, когда обрабатываются почвы или питательные среды с низкой внутренней буферной емкостью. Более того, в ирригационных схемах, которые управляли естественной жесткой водой в течение длительного времени, как это происходит в Юго-Восточной Испании, образование чешуек CaCO 3 является обычным явлением, и переход к воде с низкой щелочностью может отделить эти чешуйки, влияя на работу клапанов, фильтры и расходомеры, а также провоцируют повреждение труб.
В таблице 14.4 собраны уровни щелочности, pH и CCPP, рекомендованные Управлением водоснабжения Израиля для комбинированного сельскохозяйственного и муниципального использования, вместе с наблюдаемыми значениями в выбранных DSWP.
Таблица 14.4. Рекомендации Управления водного хозяйства Израиля по щелочности, pH и потенциалу осаждения карбоната кальция (CCPP) в DSW и их значения в выбранных SWDP
| Параметр | Израильские рекомендации по использованию ТБО в домашних и сельскохозяйственных целях [13] | Ashkelon [ 13] | Hedera [23] | Escombreras a | Águilas a |
|---|---|---|---|---|---|
| pH | & lt; 8.5 | 8,0–8,2 | 8,0–8,1 | 8,0–8,5 | 8,3–8,7 |
| Щелочность, мг л — 1 CaCO 3 | & gt; 80 | 48–52 | 85 | 50–55 | 52–60 |
| CCPP, мг L — 1 CaCO 3 | 3–10 | 0,7–1 | — | —— |
DSW, произведенные в выбранных DSWP, имеют значения pH, подходящие для использования в сельском хозяйстве, но уровни щелочности, которые обычно ниже рекомендаций Израиля (Таблица 14.4). Эти данные, вместе с отсутствием основных питательных веществ, таких как Mg 2 + , Ca 2 + и SO 4 2 — , указывают на то, что для сельскохозяйственного использования следует в целом интенсифицировать процессы последующей обработки, чтобы минимизировать агрономические проблемы и появление специфических проблем в существующих системах распределения, так как ДСВ, поставляемые с низкими значениями щелочности, довольно распространены [20,29].
torres_huesca
torres_huesca
- ЩЕЛОЧНОСТЬ: ЗДОРОВО ИЛИ ВРЕДНО?
- ОТКРЫТИЕ ЩЕЛОЧНОСТИ В НАША ШКОЛА ВОДА
- Исследовали: Кристина и Хасим
Введение
Мы проверяем щелочность в наша школьная вода, потому что нам важно понимать, что в нашей школьной воде.Щелочность важна в нашей школе вода, потому что, если вода не имеет щелочности, она с большей вероятностью кислая. Щелочность помогает воде оставаться стабильной по pH. это для нас важно пить чистую воду по соображениям здоровья, плюс мы, подростки нужна вода для нашего ежедневного рациона :). Прочтите, чтобы узнать больше о щелочность и обнаружена ли она в нашей школьной воде.
Что такое Щелочность?
Щелочность — это мера способность воды нейтрализовать кислоты или ионы водорода.Щелочность иногда может обозначаться как «Карбонатная жесткость». Щелочность действует как буфер, если были внесены какие-либо изменения в значение pH воды. Щелочность воды помогает поддерживать стабильный уровень pH. В питьевая вода и вся вода должны иметь pH 7, что означает нейтральный.
Высокая щелочность — это хорошо, если мы питьевая вода, потому что она делает воду безопасной для питья. В количество щелочности, которая должна быть в нашей воде, составляет 20-200 мг / л для обычная питьевая вода.Щелочность — это в основном растворенные минералы в вода, которая помогает нейтрализовать воду, которую мы пьем.
Откуда это взялось из?
Наибольшая щелочность в поверхностных водах происходит из карбоната кальция (CaCO3), который поступает из горных пород и почвы. Известняк содержит высокий уровень карбоната кальция. Процесс усиливается, если камни и почва уже были разбиты ранее вход в воду. Растворенные минералы попадают в воду через строительство и другие процессы
ИСТОЧНИКИ ЩЕЛОЧНОСТИ | ЧТО ПРЕДСТАВЛЯЕТСЯ НА ЭТОЙ ТАБЛИЦЕ? | |
Выщелочено из породы — известняк · Выщелочено из минералы — доломит — кальцит · Выщелочено из почвы | Это некоторые из типы минералов и горных пород, которые являются источниками щелочность |
Щелочность также защищает нашу воду от кислотного дождя.Ниже показано, как щелочность защищает pH воды и ее дикая природа.
Источник: http://euphrates.wpunj.edu/faculty/partnership/CBL/ex-cbl05.htm
Вот процедура для проверка нашей школьной воды на щелочность:
Метод определения щелочности Тестовое задание;
- Сначала необходимо заполнить трубка для титрования до линии 5 мл с водой.
- Затем положите один бромкрезол Таблетка Green-Methyl Red в воде.Закройте крышку и встряхивайте, пока планшет пропадает. Вода может стать сине-зеленой. Если вода становится розовым, вода не щелочна.
- Затем вы заполняете титрование с прямым считыванием с реагентом для тирации щелочности B. Затем заполните титр, когда плунжер доходит до нуля. отметка о выпуске. После того, как плунжер доходит до нулевой отметки отметьте, поместите титрование в центральное отверстие трубки для титрования колпачок.
- Медленно нажмите на поршень пока титруемый образец сине-зеленого цвета не изменится на розовый.Количество Реагента B, которое вводится при титровании до тех пор, пока он становится розовым — это степень щелочности воды. это измерил мои доли на миллион (ppm) из 200 ppm.
Результаты:
Школа | Количество щелочности найдено |
Школа будущего | 160 частей на миллион |
PS 11 | 140 частей на миллион |
PS 234 | 100 частей на миллион |
PS 42 | 80 страниц в минуту |
MS104 | 100 частей на миллион |
Маяк | 60.5 страниц в минуту |
PS 41 | 120 страниц в минуту |
F.I.T | 100 частей на миллион |
PS 116 | 140 частей на миллион |
I.S 131 | 😯 частей на миллион |
Что означают эти результаты иметь в виду?
Вместе с тестированием нашей школы воды мы также решили протестировать питьевую воду школ в наш район.Тест показал, что щелочность, обнаруженная в большинстве В школах Манхэттена обычно есть питьевая вода. Школа питьевой воды будущего имеет наибольшую щелочность из всех десяти школы. Это, вероятно, объясняет забавный вкус нашей воды. потому что он наполнен минералами. Beacon имеет наименьшую щелочность из всех десяти протестированных школ, но это неплохо. Вся школа вода имеет нужную щелочность.
Обсуждения
При проведении этого теста мы обнаружили что было место для ошибки или что-то, что могло сделать наш тест не точный.Возможно, мы потеряли часть пробы воды. При добавлении Реагента B к образцу, чтобы проверить, насколько щелочность в воде у нас обоих была разная интерпретация цвета розовый. Это может означать, что щелочность в вода тогда мы на самом деле думаем
Для решения этой проблемы вы можете сделать будьте осторожны с пробой воды. Решить проблему тестирования, чтобы увидеть, сколько щелочности в воде и определения если образец станет правильного розового цвета, вы должны сделать это тот же человек весь тест или одно и то же лицо, определяющее, стал розовым.
Положительная часть наличия Щелочность воды заключается в том, что она снижает чувствительность воды к кислотам. Если у вас его много в воде, значит, он наполнен минералами и может вызвать запотевание воды. Этот называется мутностью, которая может запотевать воду и делать солнечный свет очень трудно пройти. Из-за помутнения растения под водой не получать солнечный свет Без солнечного света растения не могут давать от любого кислорода и страдает дикая природа. Другое дело, что может случиться, если в воде слишком много щелочности, потому что вода становится известная как «Жесткая вода».Это может сказаться на трубах и вызвать их выделяют свинец (где применимо), который может нанести нам вред, если мы его выпьем. Когда вода становится «твердым», он для многих растворяется твердые тела. Растворенные твердые вещества — это минералы в воде. Щелочность необходима для защиты воды от кислот, как кислотный дождь. Важно понимать, что находится в нашей школьной воде! Мы надеемся, что этот тест помог вам понять состояние воды в нашей школе и др. по городу.
Руководство для инструктора — Щелочность — Роберт Б.Институт водных ресурсов Аннис (AWRI) — образование и информационно-пропагандистская деятельность
Что такое щелочность?
Щелочность — это мера способности воды нейтрализовать кислоты. Это известно как буферная способность воды или способность воды сопротивляться изменению pH при добавлении кислоты. Щелочность воды в первую очередь обусловлена наличием ионов бикарбоната, карбоната и гидроксида. Он относится к балансу углекислого газа в воде и является функцией pH.
Как измеряется щелочность?
Щелочность выражается как щелочность фенолфталеина или общая щелочность.Оба типа можно определить титрованием стандартной серной кислотой до конечной точки pH. Такие индикаторы, как фенолфталеин и бромкрезоловый зеленый-метиловый красный, определяют конечные точки, или для определения конечных точек можно использовать pH-метр. Щелочность фенолфталеина определяется титрованием до pH 8,3 и показывает общее количество гидроксида и половину присутствующего карбоната. Общую щелочность определяют титрованием до pH 5,1, 4,8, 4,5 или 3,7 в зависимости от количества присутствующего диоксида углерода. Общая щелочность включает всю карбонатно-бикарбонатную щелочность и щелочность гидроксидов.Бикарбонат — основная форма щелочности. Единица измерения щелочности — мг / л CaC03.
Какое значение имеет щелочность?
Щелочность — это мера устойчивости воды к снижению pH при добавлении в воду кислот. Кислота обычно поступает из дождя или снега, хотя в некоторых районах важны и почвенные источники. Щелочность увеличивается, поскольку вода растворяет породы, содержащие карбонат кальция, такие как кальцит и известняк.Карбонаты и гидроксид могут иметь большое значение при высокой активности водорослей и в технической воде.
Когда в озере или ручье слишком низкая щелочность, обычно ниже примерно 100 мг / л, большой приток кислот в результате сильного дождя или быстрого таяния снега может (по крайней мере временно) поглотить всю щелочность. Это приводит к падению pH воды до уровней, вредных для земноводных, рыб или зоопланктона. Озера и ручьи в районах с небольшим количеством почвы, например в горных районах, часто имеют низкую щелочность.Эти водоемы могут быть особенно чувствительны весной в периоды быстрого таяния снегов. Поскольку загрязняющие вещества имеют тенденцию вымываться из снежного покрова во время первой части таяния снега, часто бывает более высокий приток кислых загрязняющих веществ весной, что также является критическим временем для роста водных организмов. Ледниковый тилль в Великих озерах содержит породы, содержащие карбонат кальция, который помогает смягчить эффект кислотных дождей. Высокая щелочность может снизить токсичность металлов за счет использования доступных бикарбонатов и карбонатов для извлечения металла из раствора.Таким образом, металлы будут недоступны для рыб и других водных организмов.
Уход за водой в гидромассажной ванне: что такое щелочность? | Блог
Часто задаваемый вопрос, который мы слышим от владельцев гидромассажных ванн, которые пытаются сбалансировать воду, — «Что такое щелочность?». за которым часто следует: «Как мне сохранить его на нужном уровне?» В этом блоге будет рассказано, что такое щелочность воды, почему важно поддерживать ее сбалансированность и как ее регулировать.
Что такое щелочность?
Общая щелочность — это мера способности воды в гидромассажной ванне нейтрализовать кислоты.Это важная часть балансировки уровня pH, которую иногда называют «буфером», поскольку он помогает воде противостоять резким изменениям pH.
Для тех из вас, у кого есть спа Sundance в магазине Sundance Spa, общая щелочность — это третий квадрат сверху вниз на тест-полоске «6-в-1». Идеальный диапазон для общей щелочности составляет 80–120 частей на миллион (частей на миллион).
Почему это важно?
Несбалансированный щелочной уровень может отрицательно сказаться на внешнем виде воды в гидромассажной ванне (придать воде зеленый оттенок), а в некоторых случаях может вызвать сушку кожи.
Низкая щелочность — более серьезная из двух крайностей. Это может вызвать зеленую воду и быстрые колебания pH, потому что вода не может так легко противодействовать воздействию кислот, таких как кислотный дождь или естественные минералы.
Если низкие уровни щелочности не проверять в течение длительного периода времени, они могут оказать негативное влияние на поверхность вашей гидромассажной ванны, а также могут вызвать коррозию внутреннего оборудования вашей гидромассажной ванны.
Слишком высокий уровень щелочности также может привести к получению зеленой воды, поскольку он снижает эффективность дезинфицирующего средства, которое вы добавляете в воду (Sun-Boom), которое лучше всего работает в хорошо сбалансированной воде.В то время как низкая щелочность может вызвать неустойчивый pH, высокая щелочность обычно вызывает действительно высокий уровень pH.
Высокий уровень pH в воде в гидромассажной ванне может привести к накоплению кальция, что может сделать воду мутной и вызвать образование накипи (как вы можете видеть внутри своего чайника). Кальций может вызвать появление желтоватых хлопьев в воде в гидромассажной ванне и, если не принять меры, может отрицательно повлиять на работу струи и оборудование вашего спа.
Если у вас возникают проблемы с накоплением кальция, может помочь глубокая очистка водопровода вашей гидромассажной ванны.Мы рекомендуем использовать Whirlpool Rinse или Spa Marvel Cleanser, чтобы расщепить накопленный кальций в сантехнике вашего спа, и регулярно использовать Prevent II, чтобы предотвратить накопление кальция. Заходите к нам для получения дополнительной информации.
Как сбалансировать щелочность?
Общую щелочность следует поддерживать на уровне 80–120 частей на миллион. Чтобы повысить низкую щелочность и стабилизировать pH, используйте Alka-Plus. Один колпачок Alka-Plus обычно увеличивает уровень щелочности на одну клетку тест-полоски.
Лучше всего, если вы постепенно увеличиваете щелочность в течение определенного периода времени, а не добавляете большое количество химикатов сразу.Сделайте корректировку, а затем проведите еще один тест на следующий день, чтобы узнать, нужно ли добавлять в воду еще какие-либо продукты.
Для снижения высокой щелочности используйте pH Reducer. Как правило, один колпачок pH Reducer снизит уровень щелочности примерно на 1 квадрат на тест-полоске. pH Reducer следует добавлять постепенно, чтобы не допустить добавления слишком большого количества химикатов и снижения уровней до слишком низкого уровня.
Поскольку редуктор pH снижает как щелочность, так и pH, вам нужно будет проверить свой уровень pH на следующий день после корректировки щелочности, чтобы увидеть, нужно ли вам повысить уровень pH до приемлемого диапазона.Перед регулировкой pH всегда доводите уровень щелочности до приемлемого диапазона.
Если у вас все еще есть зеленый оттенок воды после того, как была отрегулирована щелочность, проверьте, соответствует ли уровень дезинфицирующего средства, который должен быть (добавьте 30 граммов, при необходимости 1 колпачок Sun-Boom).

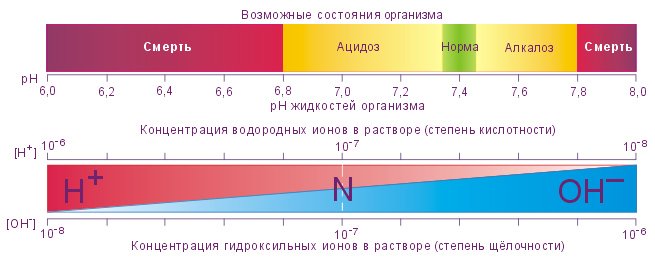 et al. The assessment of acid-base analysis: comparison of the «traditional» and the «modern» approaches // Med Glas (Zenica). 2015. Feb; 12 (1). Р. 7–18.
et al. The assessment of acid-base analysis: comparison of the «traditional» and the «modern» approaches // Med Glas (Zenica). 2015. Feb; 12 (1). Р. 7–18. Pharm. Sci. 2016, 105 (9), 2904–2912.
Pharm. Sci. 2016, 105 (9), 2904–2912.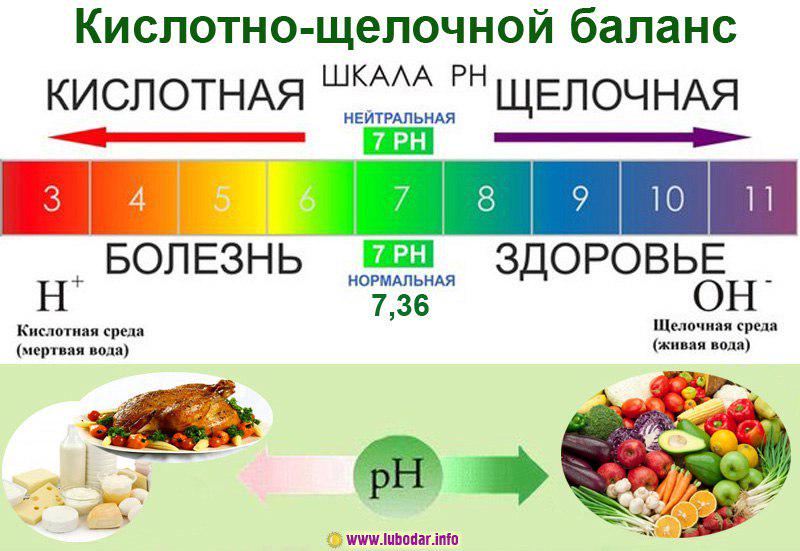 Dis. Sci. 1979, 24 (2), 101–110.
Dis. Sci. 1979, 24 (2), 101–110. 2005, Oct; 69 (10): 1985–1987.
2005, Oct; 69 (10): 1985–1987. , Nishimura T., Teruya K. et al. Protective mechanism of reduced water against alloxan-induced pancreatic beta-cell damage: Scavenging effect against reactive oxygen species // Cytotechnology. 2002, vol. 40, № 1–3, p. 139–149.
, Nishimura T., Teruya K. et al. Protective mechanism of reduced water against alloxan-induced pancreatic beta-cell damage: Scavenging effect against reactive oxygen species // Cytotechnology. 2002, vol. 40, № 1–3, p. 139–149. et al. Alkaline water improves exercise-induced metabolic acidosis and enhances anaerobic exercise performance in combat sport athletes // PLoS One. 2018, Nov 19; 13 (11).
et al. Alkaline water improves exercise-induced metabolic acidosis and enhances anaerobic exercise performance in combat sport athletes // PLoS One. 2018, Nov 19; 13 (11).