Жесткая и мягкая вода — что это значит. Виды жесткости воды
Нередко покупатели хотят узнать у нас, как у специалистов, 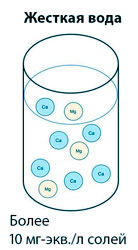 подробнее о том, что такое жесткая и мягкая вода, какие у них особенности и как смягчить воду. Мы подготовили несколько статей об этом. Надеемся, в них вы найдете ответы на большинство вопросов о жесткой и мягкой воде.
подробнее о том, что такое жесткая и мягкая вода, какие у них особенности и как смягчить воду. Мы подготовили несколько статей об этом. Надеемся, в них вы найдете ответы на большинство вопросов о жесткой и мягкой воде.
Что такое жесткая и мягкая вода?
Говоря простым языком, жесткая вода — это h3O с большим количеством растворенных в ней солей щёлочноземельных металлов, в основном, кальция и магния (а точнее, катионов Са и Mg), а мягкая — с малым их количеством. Измеряют количество так называемых «солей жесткости» в h3O в миллиграмм-эквивалентах на литр — мг-экв./л. Один мг-экв./л. означает, что в литре воды содержится 20,04 мг катионов Са или 12,16 мг катионов Mg (атомная масса, поделенная на валентность).
Классификаций жесткости воды существует несколько. В России вода считается жёсткой, если в ней более 10 мг-экв./л солей. Вода, в которой содержится от 2 до 10 мг-экв./л. солей, считается средне жесткой, а вода с концентрацией солей менее 2 мг-экв./л. считается мягкой.
Интересный факт: дождевая вода мягкая, так как перед тем, как пролиться дождем, она испарялась. В процессе парообразования «соли жесткости» не могли испаряться вместе с ней, то есть были естественным образом отфильтрованы. Жесткой вода становится, проходя через почву и собирая соли из нее.
Откуда взялись названия «жесткая» и «мягкая»
Люди издревле отмечали, что, постирав вещи в одной воде, они высыхают, оставаясь мягким, а постирав в другой — становятся грубыми, жесткими. Логично, что воду, «делающую» воду мягкими, они стаи называть мягкой, а жесткими «жесткой».
Кстати, иногда люди считают мягкую воду «живой, а жесткую «мертвой». Это неправильно. Да, такие понятия как «живая» и «мертвая» вода существуют. Конечно, они не имеют отношения к сказкам и мифам о целебности живой воды и губительности мертвой. Просто существуют теории, пока не получившие официального признания, но и не опровергнутые, что вода со щелочной реакцией имеет некоторые полезные свойства, ее и называют живой. Кислотную воду, соответственно, называют мертвой. С мягкостью или жесткостью воды это связано мало.
Почему вещи становятся жесткими после стирки в жесткой воде?
Потому, что соли забивают поры нитей, делая их менее эластичными и грубыми. Кроме того, жесткая вода придает вещам неприятный серый или желтоватый оттенок, портит их цвет. Конечно, от одной или нескольких стирок в такой воде ничего не случится, но регулярное ее использование сократит срок службы вещи и срок ее хорошего внешнего вида.
Жесткость воды бывает постоянной и временной
Гидрокарбонаты магния и кальция делают 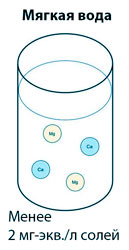 воду временно жесткой, так как распадаются при кипячении и выпадают в виде нерастворимого осадка. Накипь на дне и стенках чайника — это, чаще всего карбонаты магния и кальция, образовавшиеся из гидрокарбонатов с выделением воды и углекислого газа. Так выглядит превращение гидрокарбоната кальция: Са(НСО3)2 ——> СаСО3 + Н2О + СО2, и магния: Mg(НСО3)2 ——> MgСО3 + Н2О + СО2.
воду временно жесткой, так как распадаются при кипячении и выпадают в виде нерастворимого осадка. Накипь на дне и стенках чайника — это, чаще всего карбонаты магния и кальция, образовавшиеся из гидрокарбонатов с выделением воды и углекислого газа. Так выглядит превращение гидрокарбоната кальция: Са(НСО3)2 ——> СаСО3 + Н2О + СО2, и магния: Mg(НСО3)2 ——> MgСО3 + Н2О + СО2.
Магниевые и кальциевые соли серной, соляной, азотной и других сильных кислот не разлагаются при кипячении, h3O с большим их количеством все равно остается жесткой, отсюда и название «постоянная жесткость».
Воду с постоянной жесткостью тоже можно смягчить, и в дальнейших статьях мы расскажем, как это сделать и зачем.
Жёсткость воды, её значение и методы её устранения (стр. 1 из 3)
Федеральное агентство по образованию
Министерство образования Российской Федерации
Филиал Санкт-Петербургского государственного
инженерно-экономического университета
в г. Пскове
Кафедра математических и естественных наук
Курсовая работа
Дисциплина:
Теоретические основы прогрессивных технологий
Тема:
Жёсткость воды, её значение и методы её устранения
Псков
2007
Аннотация
Тема нашей курсовой работы затрагивает жёсткость воды, значение и методы её устранения. Мы рассмотрели особенности воды, её химические и физические свойства, дали определение жёсткости воды, описали все найденные способы устранения жёсткости, значение и последствия после её использования.
Таким образом, проведя маленькое исследование в рамках написания курсовой работы, можно понять, что жёсткая вода неблагоприятно воздействует не только на техническое и промышленное оборудование, но и на такие вещи как ткань, посуда, а также и на кожу человека и продукты питания.
Жёсткость воды – это наиболее распространённая проблема качества воды. В настоящее время для борьбы с жёсткой водой существуют и более современные способы, чем кипячение воды или вымораживание, например, установка фильтров-умягчителей. Они смягчают воду и в результате, она обладает лучшими вкусовыми качествами и более благоприятно воздействует на кожу человека.
Введение
В настоящее время всё большую актуальность приобретает проблема очистки, или правильнее сказать подготовки воды. Причём не только воды для питья и приготовления пищи, но и той, которая используется в быту — для стирки, мытья посуды и т.д. Существует проблема, общая как для загородных домов с автономной системой водоснабжения, так и для городских квартир. Имя этой проблемы — жёсткость воды. И если на качество питьевой воды жёсткость хоть и влияет, но не столь сильно, то для современной бытовой техники, автономных систем горячего водоснабжения и отопления, новейших образцов сантехники необходимость борьбы с жесткостью крайне актуальна.
Глава 1
1.1 Вода. Особенности тепловых свойств воды
Вода – одно из самых уникальных и загадочных веществ на Земле. Природа этого вещества до конца ещё не понята. Внешне вода кажется достаточно простой, в связи с чем долгое время считалась неделимым элементом. Лишь в 1766 году Г. Кавендиш (Англия) и затем в 1783 году А. Лавуазье (Франция) показали, что вода не простой химический элемент, а соединение водорода и кислорода в определённой пропорции. После этого открытия химический элемент, обозначаемый как Н, получил название «водород» (Hydrogen – от греч. hydrogenes), которое можно истолковать как «порождающий воду».
Дальнейшее исследование показали, что за незатейливой химической формулой Н2О скрывается вещество, обладающее уникальной структурой и не менее уникальными свойствами. Практически все свойства воды аномальны, а многие из них не подчиняются логике тех законов физики, которые управляют другими веществами.
Первая особенность воды: вода – единственное вещество на Земле (кроме ртути), для которого зависимость удельной теплоёмкости от температуры имеет минимум.
Из-за того, что удельная теплоёмкость воды имеет минимум около 37ºС, нормальная температура человеческого тела, состоящего на две трети из воды, находится в диапазоне температур 36-38ºС.
Вторая особенность воды: теплоёмкость воды аномально высока. Чтобы нагреть определённое её количество на один градус, необходимо затратить больше энергии, чем при нагреве других жидкостей, — по крайней мере, вдвое по отношению к простым веществам. Из этого вытекает уникальная способность воды сохранять тепло.
Третья особенность: вода обладает высокой удельной теплотой плавления, т.е. воду очень трудно заморозить, а лёд – растопить. Благодаря этому климат на Земле в целом достаточно стабилен и мягок.
Имеются особенности и в поведении объёма воды. Плотность большинства веществ – жидкостей, кристаллов и газов – при нагревании уменьшается и при охлаждении увеличивается, вплоть до процесса кристаллизации или конденсации. Плотность воды при охлаждении от 100 до 4ºС (точнее, до 3,98ºС) возрастает, как и у подавляющего большинства жидкостей. Однако, достигнув максимального значения при температуре 4ºС, плотность при дальнейшем охлаждении воды начинает уменьшаться. Другими словами, максимальная плотность воды наблюдается при температуре 4ºС (одна из уникальных аномалий воды), а не при температуре замерзания 0ºС.
Замерзание воды сопровождается скачкообразным уменьшением плотности более чем на 8% тогда как у большинства других веществ процесс кристаллизации сопровождается увеличением плотности. В связи с этим лёд (твёрдая вода) занимает больший объём, чем жидкая вода, и держится на её поверхности.
1.2 Физические свойства воды
Несмотря на свой, казалось бы, предельно простой химический состав, вода — одно из самых загадочных веществ на Земле. Достаточно упомянуть, что это единственное химическое вещество, которое существует в условиях нашей планеты одновременно в трёх агрегатных состояниях — газообразном, жидком и твердом.
Физические свойства воды своеобразны. Не совсем обычна зависимость вязкости жидкой воды от давления: в области сравнительно низких давлений при температурах до 30ºС вязкость с ростом давления уменьшается. Вода – полярная, и жидкая вода, и лёд являются диэлектриками. Вода диамагнитна. Свойства воды зависят от её изотопного состава. Так, давление пара D2O при 20ºС на 13% ниже, чем пара Н2O.
Высокая диэлектрическая проницаемость, большой дипольный момент молекулы, обеспечивающие хорошую растворимость в воде многих веществ, широкий температурный интервал существования жидкого состояния наряду с распространённостью воды обуславливают её широкое применение для многих технологических процессов.
1.3 Химические свойства воды
Вода – простейшее устойчивое химическое соединение водорода и кислорода (окись водорода — Н2O), одно из самых распространённых соединений в природе, играющее исключительно важную роль в процессах, происходящих на Земле.
Известно 3 изотопа водорода (1Н – протий; 2Н, или Д, — дейтерий; 3Н, или Т, — тритий) и 6 изотопов кислорода (14О, 15О, 16О, 17О, 18О, 19О), так что существует большое количество изотопных разновидностей молекул воды. Молекула воды представляет собой равнобедренный треугольник с ядрами О и Н в вершинах.
Химически чистая вода состоит почти исключительно из молекул Н2O. Незначительная доля молекул (при 25ºС – примерно одна на 5·109) диссоциирует по схеме Н2O ↔ Н+ + ОН—. Протон Н+ в водной среде существовать в свободном состоянии не может и, взаимодействуя с молекулами воды, образует комплексы Н5 О2+. Хотя степень диссоциации в воде ничтожна, она играет большую роль в химических процессах, происходящих в различных системах, в том числе и биологических. В частности, она является причиной гидролиза солей слабых кислот и оснований и некоторых других реакций, протекающих в воде.
Вода взаимодействует со многими элементами и веществами. Так, при реакции воды с наиболее активными металлами выделяется водород и образуется соответствующая гидроокись. При реакции со многими окислами образуются кислоты или основания. Вода гидролизует гидриды и карбиды щелочных и щелочноземельных металлов и другие вещества.
Глава 2. Жёсткость воды и методы её устранения
2.1 Определение жёсткости воды
Природная вода обязательно содержит растворённые соли и газы (кислород, азот и др.). Присутствие в воде ионов Mg2+ и Са2+ и некоторых других, способных образовывать твёрдые осадки при взаимодействии с анионами жизненных органических кислот, входящих в состав различных мыл (например, со стеарат-ионом С17Н35СОО2-), обуславливает так называемую жёсткость воды.
Во всех просмотренных нами научных источниках, понятие жёсткости воды обычно связано с катионами кальция (Са2+) и в меньшей степени магния (Mg2+). В действительности, все двухвалентные катионы в той или иной степени влияют на жёсткость. Они взаимодействуют с анионами, образуя соединения (соли жёсткости) способные выпадать в осадок. Одновалентные катионы (например, натрий Na+) таким свойством не обладают.
В данной таблице приведены основные катионы металлов, вызывающие жёсткость, и главные анионы, с которыми они ассоциируются:
На практике стронций, железо и марганец оказывают на жёсткость столь небольшое влияние, что ими, как правило, пренебрегают. Алюминий (Al3+) и трёхвалентное железо (Fe3+) также влияют на жёсткость, но при уровнях рН, встречающихся в природных водах, их растворимость и, соответственно, «вклад» в жёсткость ничтожно малы. Аналогично, не учитывается и незначительное влияние бария (Ва2+).
Чем выше концентрация указанных двухзарядовых катионов Mg2+ и Са2+ в воде, тем вода жёстче. Наличие в воде этих катионов приводит к тому, что при использовании, например при стирке, обычного мыла (но не синтетического моющего средства) часть его расходуется на образование с этими катионами нерастворимых в воде соединений так называемых жирных кислот (мыло представляет собой смесь натриевых и калиевых солей этих кислот):
2.3 Значение жёсткости воды
Как мы уже говорили, жёсткость воды определяется содержанием в воде растворенных солей кальция и магния, которые при нагревании выпадают в осадок, образуя налёт, всем хорошо известный как накипь. Сравнительно безобидная на стенках чайника накипь может стать причиной преждевременного выхода из строя сантехники, посудомоечных и стиральных машин (недаром дорогие модели бытовой техники снабжены встроенными умягчителями).
Накипь может стать причиной преждевременного выхода из строя сантехники, посудомоечных и стиральных машин
На бытовом же уровне жёсткость проявляет себя значительным (на 30-50%) перерасходом моющих средств при стирке белья и умывании, а также ухудшением потребительских свойств воды. При кипячении достаточно жёсткой воды на её поверхности образуется плёнка, а сама вода приобретает характерный привкус. При заваривании чая или кофе в такой воде может выпадать бурый осадок, теряется вкусовые качества чая. В жёсткой воде с трудом развариваются пищевые продукты, а сваренные в ней овощи невкусны. К тому же диетологами установлено, что в жёсткой воде хуже разваривается мясо. Связано это с тем, что соли жёсткости вступают в реакцию с животными белками, образуя нерастворимые соединения. Это приводит к снижению усвояемости белков.
С точки зрения применения воды для питьевых нужд, её приемлемость по степени жёсткости может существенно варьироваться в зависимости от местных условий. Порог вкуса для иона кальция в диапазоне 2-6 мг-экв/л, в зависимости от соответствующего аниона, а порог вкуса для магния и того ниже. В некоторых случаях для потребителей приемлема вода с жёсткостью выше 10 мг-экв/л. Высокая жёсткость ухудшает органолептические свойства воды, придавая ей горьковатый вкус.
Всемирная Организация Здравоохранения не предлагает какой-либо рекомендуемой величины жёсткости по показаниям влияния на здоровье. В материалах ВОЗ говорится о том, что хотя ряд исследований и выявил статистически обратную зависимость между жёсткостью питьевой воды и сердечно-сосудистыми заболеваниями, имеющиеся данные не достаточны для вывода о причинном характере этой связи. Аналогичным образом, однозначно не доказано, что мягкая вода оказывает отрицательный эффект на баланс минеральных веществ в организме человека.
Вместе с тем, в зависимости от рН и щелочности, вода с жёсткостью выше 4 мг-экв/л может вызвать в распределительной системе отложение шлаков и накипи (карбоната кальция), особенно при нагревании. Именно поэтому нормами Котлонадзора вводятся очень строгие требования к величине жёсткости воды, используемой для питания котлов (0.05-0.1 мг-экв/л).
К сожалению, далеко не всем известно также о неблагоприятном влиянии жёсткости на здоровье человека при умывании.
Связано это с тем, что при взаимодействии солей жёсткости с моющими веществами (мыло, стиральные порошки, шампуни) может происходить образование нерастворимых «мыльных шлаков» в виде пены. Такая пена после высыхания остается в виде налета на сантехнике, белье, человеческой коже, на волосах (неприятное чувство «жёстких» волос хорошо известное многим). При этом разрушается естественная жировая плёнка, которой всегда покрыты здоровые волосы и нормальная кожа, забиваются поры, появляются сухость, шелушение, перхоть. Первым тревожным признаком такого негативного воздействия является характерный «скрип» чисто вымытой кожи или волос. Оказывается, что вызывающее у некоторых людей раздражение чувство «мылкости» после пользования мягкой водой, является признаком того, что защитная жировая плёнка на коже цела и невредима. Именно она-то и скользит. В противном случае, приходится пользоваться лосьонами, умягчающими и увлажняющими кремами, необходимые для восстановление защиты. Недаром косметологи рекомендуют использовать для умывания очень мягкую дождевую или талую воду.
Как мы уже говорили, «мыльные шлаки» в виде пены, высыхая, остаётся на сантехнике, белье и т.д. В результате, ткань становится грубой и неэластичной; она перестаёт пропускать воздух и влагу. Портится и внешний вид изделия: ткань приобретает серо-жёлтый оттенок, блекнут краски рисунка. Осевшие на ткани «известковые мыла» лишают её прочности.
Вместе с тем, необходимо упомянуть и о другой стороне медали. Мягкая вода с жёсткостью менее 2 мг-экв/л имеет низкую буферную ёмкость (щёлочность) и может, в зависимости от уровня рН и ряда других факторов, оказывать повышенное коррозионное воздействие на водопроводные трубы. Поэтому, в ряде применений (особенно в теплотехнике) иногда приходится проводить специальную обработку воды с целью достижения оптимального соотношения между жёсткостью воды и её коррозионной активностью
Жёсткость воды, её значение и методы её устранения (стр. 2 из 3)
2С17 Н35 СОО— + Са2+ = (С17Н 35СОО)2Са↓
2С17Н 35 СОО— + Мg2+ = (С17Н 35СОО)2Mg↓
и пена образуется лишь после полного осаждения ионов.
Мыла – это натриевые (иногда калиевые) соли органических кислот, и их состав можно условно выразить формулой NaR или KR, где R – кислотный остаток. Анионы R образуют с катионами кальция и магния нерастворимые соли CaR2 и MgR2 . На образование этих нерастворимых солей и расходуется бесполезно мыло. Таким образом, при помощи мыльного раствора мы можем оценить общую жёсткость воды, общее содержание в ней ионов кальция и магния.
Ионы кальция (Ca2+) и магния (Mg2+), а также других щёлочноземельных металлов, обуславливающих жёсткость, присутствуют во всех минерализованных водах. Их источником являются природные залежи известняков, гипса и доломитов. Ионы кальция и магния поступают в воду в результате взаимодействия растворённого диоксида углерода с минералами и при других процессах растворения и химического выветривания горных пород. Источником этих ионов могут служить также микробиологические процессы, протекающие в почвах на площади водосбора, в донных отложениях, а также сточные воды различных предприятий. В маломинерализованных водах больше всего ионов кальция. С увеличением степени минерализации содержание ионов кальция быстро падает и редко превышает 1 г/л. Содержание же ионов магния в минерализованных водах может достигать нескольких граммов, а в солёных водах нескольких десятков граммов.
В целом, жёсткость поверхностных вод, как правило, меньше жёсткости вод подземных. Жёсткость поверхностных вод подвержена заметным сезонным колебаниям, достигая обычно наибольшего значения в конце зимы и наименьшего в период половодья, когда обильно разбавляется мягкой дождевой и талой водой.
Жёсткость — это особые свойства воды, во многом определяющие её потребительские качества и потому имеющие важное хозяйственное значение.
Для тушения пожаров, полива огорода, уборки улиц и тротуаров жёсткость воды не имеет принципиального значения. Но в ряде случаев жёсткость воды может создать проблемы. При принятии ванны, мытье посуды, стирке, мытье машины жёсткая вода гораздо менее эффективна, чем мягкая. Это обуславливается некоторыми фактами:
· При использовании мягкой воды расходуется в 2 раза меньше моющих средств;
· Жёсткая вода, взаимодействуя с мылом, образует “мыльные шлаки”, которые не смываются водой и оставляют малосимпатичные разводы на посуде и поверхности сантехники;
· Во многих промышленных процессах соли жёсткости могут вступить в химическую реакцию, образовав нежелательные промежуточные продукты.
Жёсткая вода образует накипь на стенках нагревательных котлов, батареях, чем существенно ухудшает их теплотехнические характеристики. Накипь является причиной 90% отказов водонагревательного оборудования. Поэтому к воде, подвергаемой нагреву в котлах, бойлерах и т.п. предъявляются на порядок более высокие требования по жесткости. Тонкий слой накипи на греющей поверхности вовсе не безобиден, так как продолжительность нагревания через слой накипи, обладающей малой теплопроводностью, постепенно возрастает, дно прогорает все быстрее и быстрее – ведь металл охлаждается с каждым разом все медленнее и медленнее, долго находится в прогретом состоянии. В конце концов, может случиться так, что дно сосуда не выдержит и начнёт протекать. Этот факт очень опасен в промышленности, где существуют паровые котлы.
Жёсткая вода мало пригодна для стирки. Накипь на нагревателях стиральных машин выводит их из строя, она ухудшает ещё и моющие свойства мыла. Катионы Ca2+ и Mg2+ реагируют с жирными кислотами мыла, образуя малорастворимые соли, которые создают плёнки и осадки, в итоге снижая качество стирки и повышая расход моющего средства. А при стирке тканей жёсткой водой образующиеся нерастворимые соединения осаждаются на поверхности нитей и постепенно разрушают волокна.
Различают временную и постоянную жёсткость воды. Обусловлено это различие типом анионов, которые присутствуют в растворе в качестве противовеса кальцию и магнию.
Временная жёсткость воды обусловлена наличием в воде гидрокарбонатов, например, гидрокарбоната кальция Ca(HCO3)2 и магния Mg(HCO3)2.
При кипячении воды гидрокарбонаты разлагаются с образованием осадка среднего или основного карбоната:
Ca(HCO3)2 = СаСО3 ↓+ СО2↑+ Н2О,
Mg(HCO3)2 = Мg2 (ОН) 2 СО3↓ + 3СО2↑ + Н2О,
и жёсткость воды снижается. Поэтому гидрокарбонатную жёсткость называют временной.
Остальная часть жёсткости, сохранившаяся после кипячения воды, называется постоянной жёсткостью(или некарбонатная). Она обусловлена присутствием в ней сульфатов, хлоридов и других растворимых соединений кальция и магния, которые хорошо растворимы и так просто не удаляются.
Также различают и общую жёсткость воды. Она определяется суммарной концентрацией ионов кальция и магния. Представляет собой сумму карбонатной (временной) и некарбонатной (постоянной) жёсткости.
Жёсткость воды измеряется в миллиграммах эквивалент на литр (м-экв/л). Обычно, жёсткой вода считается с жёсткостью 1 м-эвк/л и более.
Классификация воды по жёсткости
Особенно большой жёсткостью отличается вода морей и океанов. Так, например, кальциевая жёсткость воды в Чёрном море составляет 12 мг-экв/л, магниевая – 53,5 мг-экв/л, а общая – 65,5 мг-экв/л. В океанах же средняя кальциевая жёсткость равняется 22,5 мг-экв/л, магниевая – 108 мг-экв/л, а общая – 130,5 мг-экв/л.
2.2 Методы устранения жёсткости воды
Для избавления от временной жёсткости необходимо просто вскипятить воду. При кипячении воды гидрокарбонаты разлагаются с образованием осадка среднего или основного карбоната:
Ca(HCO3)2 = СаСО3 ↓+ СО2↑+ Н2О,
Mg(HCO3)2 = Мg2 (ОН) 2 СО3↓ +3СО2↑ + Н2О,
и жёсткость воды снижается. Поэтому гидрокарбонатную жёсткость называют временной.
С ионами железа реакция протекает сложнее из-за того, что FeCO3 неустойчивое в воде вещество. В присутствии кислорода конечным продуктом цепочки реакций оказывается Fe(OH)3, представляющий собой темно-рыжий осадок. Поэтому, чем больше в воде железа, тем сильнее окраска у накипи, которая осаждается на стенках и дне сосуда при кипячении.
Умягчить жёсткую воду можно и обработкой воды различными химическими веществами. Так, временную (карбонатную) жёсткость можно устранить добавлением гашеной извести:
Са2+ +2НСО—3 + Са2+ + 2ОН— = 2СаСО3↓+ 2Н2О
Mg2+ +2НСО—3 + Са2+ + 4ОН— = Mg(ОН) 2↓+2СаСО3↓+ 2Н2О.
При одновременном добавление извести и соды можно избавиться от карбонатной и некарбонатной жёсткости (известково-содовый способ). Карбонатная жёсткость при этом устраняется известью (см. выше), а некарбонатная – содой:
Са2+ + СО2-3 = СаСО3↓
Mg2+ + СО2-3 = Mg СО3
и далее
Mg СО3 + Са2+ + 2ОН— = Mg(ОН) 2↓+СаСО3↓
Вообще, с постоянной жёсткостью бороться труднее. Кипячение воды в данном случае не приводит к снижению её жёсткости.
Для борьбы с постоянной жёсткостью воды используют такой метод, как вымораживание льда. Необходимо просто постепенно замораживать воду. Когда останется примерно 10 % жидкости от первоначального количества, необходимо слить не замершую воду, а лёд превратить обратно в воду. Все соли, которые образую жёсткость, остаются в не замершей воде.
Ещё один способ борьбы с постоянной жёсткостью – перегонка, т.е. испарение воды с последующей её конденсацией. Так как соли относятся к нелетучим соединениям, то они остаются, а вода испаряется.
Также, чтобы избавиться от постоянной жёсткости, можно, например, к воде добавить соду:
СаСl2 + Na2CO3 = CaCO3 ↓+ 2NaCl.
Также известны методы обработки воды (магнитное и электромагнитное воздействие, добавление полифосфатов или других «антинакипинов»), позволяющие на время «связать» соли жёсткости, не давая им в течение какого-то времени выпасть в виде накипи. Однако эти методы не нейтрализуют соли жёсткости химически и поэтому нашли ограниченное применение в водоподготовке технической воды. Единственным же экономически оправданным методом удаления из воды солей жёсткости является применение ионообменных смол. Пропуская воду через слой специального реагента – ионообменной смолы (ионита), ионы кальция, магния или железа переходят в состав смолы, а из смолы в раствор переходят ионы Н+ или Na+, и вода умягчается, её жёсткость снижается.
Но такие методы, как замораживание и перегонка, пригодны только для смягчения небольшого количества воды. Промышленность имеет дело с тоннами. Поэтому для устранения жёсткости в данном случае принимается современный метод устранения – катионный. Этот способ основан на применении специальных реагентов – катионитов, которые загружаются в фильтры и при пропускании через них воды, заменяют катионы кальция и магния на катион натрия. Катиониты – синтетические ионообменные смолы и алюмосиликаты.
Как определить жесткость воды

Как определить жесткость воды
С первого взгляда такое понятие, как жесткость воды, звучит странно – если бы речь шла о льде, тогда было бы все значительно понятнее. Но на самом деле этой характеристике уделяется большое внимание достаточно часто и в разных сферах, так как вода влияет на здоровье человека. Ниже мы ответим на вопрос, как именно и какие методы нужно использовать для того, чтобы определять жесткость воды.
Из этой статьи вы узнаете:
-
Как определить жесткость воды
-
Как определить жесткость воды с помощью приборов
-
Как определить жесткость воды в домашних условиях
-
Какие соли определяют жесткость воды
Для чего необходимо определять жесткость воды
Такой показатель, как жесткость воды, напрямую зависит от того, какое количество солей кальция и магния в ней содержится. Жесткость воды – неоднозначное понятие, так как она может быть сульфатной или карбонатной, это можно определить разными способами.
|
Временная жесткость |
Карбонатная жесткость |
|
Кальций |
Гидрокарбонат |
|
Магний |
Сульфат |
|
Стронций |
Хлорид |
|
Железо |
Нитрат |
|
Марганец |
Силикат |
По своей сути, жесткость воды – это положительно заряженные ионы кальция и магния, которые в ней растворены. Определить этот показатель можно следующим образом: если его значение высокое, то при нагреве емкости с водой на ее стенках появится налет от солей.
Человек тоже подвержен появлению подобного налета, но проявляется он совершенно по-другому: камнями в желчном пузыре, почках или печени. Определить жесткость воды важно, поскольку от этого значения зависит возможность дальнейшего использования жидкости в той или иной сфере.
У вас должны возникнуть вопросы о жесткости воды дома или в офисе в том случае, если на чайнике появилась накипь, плохо работает бойлер, стиральная машина некачественно стирает. В таких ситуациях будет полезным определить значение этого показателя, например, сдав пробу на анализ в лабораторию.
Как определить жесткость воды различного типа
Как определить карбонатную и некарбонатную жесткость воды
Карбонатная жесткость – это почти 100 % всех случаев, но для того, чтобы определить, что это именно она, нужно использовать специальные методы.
Что можно сделать, чтобы определить карбонатную жесткость воды:
-
произвести химическое исследование на жесткость;
-
обратиться в лабораторию;
-
купить в магазине специальный тест, который позволит определить жесткость воды;
-
обратиться за помощью к специалистам.

Статьи, рекомендуемые к прочтению:
Как определить временную жесткость воды
Наличие временной жесткости воды характеризуется наличием в ее составе положительно заряженных ионов кальция, магния и железа, бикарбонатных и гидрокарбонатных анионов (II). Ее можно определить следующим образом: при нагреве такой воды происходит разложение гидрокарбонатов, но образуются малорастворимый карбонатный осадок, вода и углекислый газ.
Как определить постоянную жесткость воды
Для того чтобы определить постоянную жесткость воды, нужно выявить содержание в ней солей кальция и магния – сульфатов, фосфатов и хлоридов, которые полностью растворяются в воде и не осаждаются при кипячении. Воду можно очистить от них фильтрами с ионообменной смолой, обратным осмосом или электродиализом. Чтобы определить показатель общей жесткости воды, нужно суммировать показатели временной и постоянной жесткости.

Как определить жесткость воды в лаборатории
Как определить жесткость воды с помощью специальных приборов
Вода должна иметь оптимальный показатель жесткости, поскольку полное отсутствие солей вредно для организма человека. Если в воде, например, мало карбонатных солей, это ведет к появлению сердечнососудистых заболеваний.
Если говорить о самих емкостях, в которых вода нагревается, то мягкая вода способствует коррозии. Поэтому после работы оборудования с мягкой водой в теплоэнергетике поверхности дополнительно обрабатывают раствором, содержащим вещества, которые замедляют этот процесс.
Таким образом, вода, из какого источника вы бы ее ни взяли, имеет какой-то показатель жесткости, причем идеально, если он имеет среднее значение, ведь как избыток солей, так и их недостаток ведут к определенным последствиям.

Определить жесткость воды в наше время несложно – сейчас можно приобрести специальные приспособления для контроля этого показателя и в доме, и на производстве. Оптимальный вариант – прибор TDS-3, на рынке его можно встретить под разными торговыми названиями.

Можно использовать другое приспособление, которое позволяет определить жесткость воды, –электролизер. Это достаточно дешевый прибор.

Электорлизер не сможет определить уровень жесткости воды в цифрах, но он окрасит жидкость в определенный цвет в зависимости от того, насколько в ней много соли. После электролиза вы поймете, с какими именно примесями имеете дело также по цвету воды.
Подобный прибор вы можете изготовить сами, для этого возьмите:
-
нержавеющую сталь, размер 50 х 50 см;
-
болты М6 х 150;
-
шайбы;
-
гайки;
-
прозрачную трубку;
-
штуцеры;
-
пластиковый контейнер объемом полтора литра;
-
фильтр для очистки воды;
-
обратный клапан для воды.
Основой для будущего прибора будет служить лист нержавейки, идеально — AISI 316L, если она импортная, и 03Х16Н15М3, если она отечественная.
Теперь нержавейку нужно разметить и разрезать на 16 одинаковых квадратов, после чего у каждого из них срезаем один угол, а на противоположном углу сверлим дырку, которая пригодится чуть позже. Принцип работы электролизера заключается в движении электричества от пластины одного заряда к пластине противоположного заряда, как итог – вода распадается на кислород и водород.

Для того чтобы создать хорошее движение тока, пластины подключают поочередно: сначала положительный заряд, затем отрицательный, снова положительный и т. д. Трубка применяется для изоляции, от нее нужно отрезать кольцо, разрезав которое получаем полоску толщиной 1 мм.
Шайбы нужны для того, чтобы собрать пластины: на болт прикручиваем шайбу, потом пластину и три шайбы, потом снова пластина и так далее. На каждом заряде должно быть по восемь пластин. Все это нужно делать достаточно аккуратно, чтобы избежать соприкосновения спилов пластин с электродами.
Следующий этап создания прибора для определения качества воды – стягивание гаек и изоляция пластин, после чего помещаем то, что получилось, в пластмассовый контейнер подходящего размера.
В местах касания болтами стен бокса сверлим две дыры. Может получиться так, что болты не проходят в ёмкость, тогда обрежьте их и затяните для герметичности гайками. Теперь сверлим отверстие в крышке для штуцеров. Для создания герметичности шва обрабатываем его силиконовым герметиком.
До того как вы соберетесь определить жесткость воды таким прибором, нужно проверить, достаточно ли хорошо он работает: подключите прибор к питанию, наполните водой до болтов, накройте крышкой, подключите к штуцеру трубку и опустите другой конец трубки в воду. Если ток появится, то его можно увидеть.
Теперь ток постепенно нужно увеличивать. Дистиллированная вода из-за своей чистоты очень плохо проводит ток, поэтому для создания электролита в нее нужно добавить щелочь, например, гидроксид натрия (присутствует в средствах для очистки труб типа «Крот»). Защитный клапан предотвращает излишнее скопление газов. Поздравляем, у вас есть собственноручно изготовленный прибор, который позволит определить жесткость воды!
Как определить жесткость воды с помощью мыла
Этот способ был описан И. Шереметьевым. В его основе лежит трудность размыливания хозяйственного мыла в жесткой воде. Мыльная пена появляется в том случае, когда мыло свяжет избыток солей кальция и магния.
Определить жесткость воды этим способом можно таким образом: берем 1г хозяйственного мыла, измельчаем и постепенно, аккуратно, избегая появления пены, растворяем его в небольшом количестве горячей дистиллированной воды.
Полученный раствор переливаем в цилиндрический стакан, теперь в него нужно долить дистиллированной воды до уровня 6 см, если мыло 60 %,или до уровня 7 см, если мыло 72 % (этот процент указан на самом куске мыла). На каждый сантиметр имеющегося раствора приходится такое количество мыла, которое может связать соли жесткости, их содержится 1°dH на 1 л. воды. Теперь берем литровую банку и наполовину заполняем ее той водой, жесткость которой хотим определить. Затем при постоянном помешивании постепенно льем туда приготовленный раствор. Сначала будут видны только темные хлопья, а потом появятся цветные пузыри. Если образуется плотная белая пена, то это говорит о том, что все соли жесткости в исследуемой воде связаны. Теперь нужно посчитать, сколько сантиметров из приготовленного раствора мы вылили – каждый сантиметр связал в половине литра воды количество солей, соответствующее 2°dH, то есть если для получения пены пришлось добавить 4 см мыльного раствора, то жесткость исследуемой воды равна 8°dH.
В том случае если раствор уже закончился, а пены так и нет, мы имеем дело с жесткостью воды, превышающей 12°dH. Тогда, чтобы определить искомое значение, повторяем опыт, но исследуемую воду разбавляем дистиллированной водой в два раза. Тот результат, который получим в итоге повторного анализа, следует умножить на два, это и будет искомым показателем жесткости воды.
Обычные стаканы, как правило, имеют примерно такие параметры: объем – 200–250 мл, высота –10 см, нижний диаметр – 55 мм и более, верхний диаметр – 73 мм. Таким образом, его средний диаметр составляет примерно 63 мм. Наиболее точно определить жесткость воды у вас получится в том случае, если вы будете использовать химический цилиндрический стакан с диаметром около 6 см. Конечно, можно использовать и конусный стакан, но тогда погрешность будет большей. Хочется отметить, что абсолютной точности измерения от этого способа ждать не стоит, но точности 1–2 °dH вполне достаточно для определения состояния воды. Такая погрешность является в большей мере следствием разности верхнего и нижнего диаметров сосуда, в котором находится мыльный раствор, а также на нее влияют качество мыла, дистиллированной воды и ваш опыт осуществления данного анализа.
Этот метод очень простой и позволяет самостоятельно определить жесткость воды, поэтому такая небольшая погрешность при определении этого показателя не должна заставлять вас отказываться от его применения.
Как еще определить жесткость воды в домашних условиях
На самом деле определить жесткость воды несложно. Если вам нужно узнать точную цифру, вы всегда можете отнести пробу на анализ в лабораторию. Наиболее оптимальный способ определить жесткость воды – провести тест, используя реактив Трилон Б. Также возможно получить быстрые результаты, применив специальное оборудование, минимальная стоимость которого 10–15 у.е. Это небольшие деньги, если необходимо часто контролировать этот показатель дома.
Если у вас нет этого оборудования, но вам нужно прямо сейчас определить жесткость воды, можете воспользоваться следующим способом. Просто возьмите кусок мыла и умойтесь с ним – если пены нет и сушится кожа, при этом на лейке душа или в чайнике имеется налет, то вода жесткая. Если все наоборот, то вода мягкая или средней жесткости.
На самом деле существуют еще некоторые способы, которые позволят определить показатель жесткости:
-
Наиболее доступный метод предполагает определить качество воды по внешнему виду и вкусу. В идеале она прозрачная, не имеет осадка и постороннего запаха.
-
Чтобы определить, насколько вода чистая, ее нужно налить в прозрачный чистый стакан на 20 см и поставить на лист с текстом. Если сквозь воду текст получится прочитать, то этот показатель в норме.
-
Цвет воды можно определить подобным образом, только налить нужно 100 мл воды в стакан и поставить его на белую бумагу. Если в воде присутствуют примеси органики, жидкость темнеет.
-
По запаху можно определить чистоту жидкости. Нагрейте воду до 20°С, затем – до 60°С. Если вы замечаете неприятный гнилостный запах, значит, в ней есть примеси сероводорода.
-
Вкус также позволяет определить некоторые качества. Для этого налейте воду в чистую посуду, прокипятите небольшой объем воды в течение пяти минут, после чего остудите до 20°С–25°С, теперь попробуйте. Сладковатый вкус свидетельствует о содержании в ней гипса, горький – соли магния, терпкий – соли железа. Гнилостный вкус появляется от попадания в воду растительных или животных организмов. Профильтровав, можно определить наличие твердых примесей, но предварительно воду нужно отстоять в течение некоторого времени.
-
Попробуйте капнуть воду на стекло или зеркало. После того как жидкость испарится, изучите поверхность: если она осталась чистой – вода также чистая. Наличие пятен – явный признак плохого качества воды. Присмотритесь к аквариуму, если он у вас есть, его обитатели обычно очень чувствительны к качеству воды.
Вышеприведенные способы не позволят точно определить жесткость и качество воды, поэтому лучше всего обратиться к специалистам.
Если нужно определить жесткость воды для дома, дачи или коттеджа, лучше всего сделать анализ, так как количество магния и кальция может быть в ней любое в зависимости от множества факторов.
Вы потратите деньги на анализ, но будете точно знать, насколько эффективным окажется приобретённый фильтр.
Существует большое количество российских компаний, разрабатывающих системы водоочистки. Положившись только на себя, выбрать нужный фильтр затруднительно. Сделать дома очистную систему самим, даже если вы предварительно немного почитаете об этом, не будет достаточно эффективным способом очистки.
Надежнее обратиться в компанию по установке фильтров, которая предоставляет полный спектр услуг: консультацию специалиста, анализ воды из скважины или колодца, подбор подходящего оборудования, доставку и подключение системы. Кроме того, важно, чтобы компания предоставляла и сервисное обслуживание фильтров.
Таковой является компания Biokit, которая предлагает широкий выбор систем обратного осмоса, фильтры для воды и другое оборудование, способное вернуть воде из-под крана ее естественные характеристики.
Специалисты нашей компании готовы помочь вам:
-
подключить систему фильтрации самостоятельно;
-
разобраться с процессом выбора фильтров для воды;
-
подобрать сменные материалы;
-
устранить неполадки или решить проблемы с привлечением специалистов-монтажников;
-
найти ответы на интересующие вопросы в телефонном режиме.
Доверьте очистку воды системам от Biokit – пусть ваша семья будет здоровой!
Какая жесткость воды в москве — MOREREMONTA
Одним из наиболее часто задаваемых вопросов жителями города Москвы является вопрос о величине жесткости питьевой воды. Это обусловлено широким распространением в быту посудомоечных и стиральных машин, для которых расчет загрузки моющих средств осуществляется исходя из фактического значения жесткости используемой воды.
Узнать значение жесткости воды по своему адресу вы можете с помощью нашего электронного сервиса «Качество воды в районах Москвы».
В России жесткость измеряют в «градусах жесткости», а мировые производители используют принятые в своих странах единицы измерения. Поэтому для удобства жителей создан «Калькулятор жесткости», с помощью которого можно перевести значения жесткости из одной системы измерения в другую, чтобы правильно настроить свою бытовую технику.
| Показатель жесткости | Текущая ед.измерения | Требуемая ед.измерения | Результат расчета показателя |
|---|---|---|---|
Жесткостью называют совокупность свойств воды, связанных с содержанием в ней растворённых солей, главным образом, кальция и магния («солей жесткости»). Общая жесткость складывается из временной и постоянной. Временную жесткость можно устранить кипячением воды, что обусловлено свойством некоторых солей выпадать в осадок, образуя так называемую накипь.
Основной фактор, влияющий на величину жесткости – растворение горных пород, содержащих кальций и магний (известняки, доломиты), при прохождении через них природной воды. Поверхностные воды, в целом, более мягкие, чем подземные. Жесткость поверхностных вод подвержена заметным сезонным колебаниям, достигая максимума в зимний период. Минимальные величины жесткости типичны для периодов половодья или паводка, когда происходит интенсивное поступление в источники водоснабжения мягких талых или дождевых вод.
Единицы измерения жесткости
В России жесткость измеряют в «градусах жесткости» (1°Ж = 1 мг-экв/л = 1/2 моль/м3). За рубежом приняты другие единицы измерения жесткости воды.
Чтобы с успехом долгое время эксплуатировать посудомоечную машину необходимо очень тщательно изучить инструкцию и соблюдать ее неукоснительно. Прежде всего, нужно подумать о качестве воды, которая поступает в посудомойку. Сегодня мы бы хотели поговорить об уровне жесткости воды в Москве. Насколько подаваемая в дома вода подходит для посудомоечных машин? Ведь если вода очень жесткая, то даже ионообменник не справится с ее умягчением и возникнут проблемы. В общем будем разбираться.
Показатели в разных административных округах
Наверное, правильнее было бы привести показатели жесткости воды по районам Москвы, но в этом случае статья получится чересчур громоздкой. Да и смысла в этом особого нет, поскольку разница между несколькими смежными районами будет невелика. Приведем показатели жесткости воды по административным округам г. Москвы.
- Центральный – 0 Ж средний показатель составляет 3,3.
- Северный – 0 Ж в среднем 3,6.
- Северо-Восточный – 0 Ж в среднем 3,4.
- Восточный – 0 Ж в среднем 3.
- Юго-Восточный – 0 Ж около 3,2.
- Южный – 0 Ж около 3,5.
- Юго-Западный – 0 Ж в среднем 3,4.
- Западный – 0 Ж около 3,5.
- Северо-Западный – 0 Ж около 3,1.
- Зеленоградский – 0 Ж около 3,5.
- Троицкий – 0 Ж около 3,2.
- Новомосковский – 0 Ж около 3,1.
Троицкий и Новомосковский административные округа очень большие, поэтому разбег жесткости воды там от 3,1 до 3,4 0 Ж.
Если вы хотите получить более точную информацию о текущем значении жесткости воды по вашему адресу, вы можете посетить сайт Мосводоканала. На сайте в разделе «Населению» есть подраздел «Качество воды в районах Москвы». Заходите в этот подраздел и вводите над картой свой домашний адрес. Ниже в таблице, кроме прочего, появится текущий показатель жесткости воды.
Изменения показателей
Не зря Мосводоканал организовал для населения г. Москвы возможность отслеживать состояние поступающей к ним в дома воды в режиме онлайн. Основные показатели постоянно меняются, поэтому недостаточно посмотреть их один раз, их необходимо отслеживать. Почему показатели жесткости меняются? Причин довольно много, но основные изменения происходят при смене времен года.
Зимой вода наиболее жесткая. Именно зимой в неблагополучных, с точки зрения качества воды, районах посудомоечные и стиральные машины подвергаются наибольшей опасности. Весной вода в водопроводе становится значительно мягче из-за поступления в водоемы большого количества талых и дождевых вод. Летом показатели тоже могут меняться, но незначительно, а вот осенью в дождливую пору, вода на некоторое время умягчается и остается мягче нормы до первых морозов.
Жесткость воды для посудомоечной машины довольно легко отследить, если ты живешь в пределах МКАД. Поможет сайт Мосводоканала. Людям, которые живут далеко от Москвы, такая услуга недоступна, поэтому узнавать жесткость воды для посудомойки им придется самостоятельно.
Какие показатели считаются нормальными
Нам осталось выяснить, насколько жесткую воду способна выдержать посудомоечная машина. Иными словами, какие существуют допустимые значения 0 Ж для бытовых посудомоечных машин. Чтобы узнать эти значения, достаточно открыть инструкцию к своей посудомоечной машины, но проблема в том, что производитель может указать значения не в градусах жесткости 0 Ж, а в других единицах измерения:
Заниматься переводом показателей жесткости воды из одних единиц в другие довольно утомительно, да и не факт, что вы сделаете это правильно. На помощь снова придет сайт Мосводоканала. Заходим в раздел «Населению», а затем в подраздел «Калькулятор жесткости воды». К примеру, по инструкции нормальный показатель жесткости для ПММ составляет 9 0 DH. Вводим 9 в левую строчку калькулятора. В столбце «Текущая единица измерения» выбираем 0 DH. В столбце «Требуемая единица измерения» выбираем 0 Ж. В строчке «Результат расчета показателя» появится результат. В нашем случае 9 0 DH = 3,2 0 Ж.
Остается позвонить в водоснабжающую организацию вашего города и узнать текущий уровень жесткости воды. Такая информация общедоступна, никто от вас ее скрывать не будет. Простое сравнение полученных показателей подскажет вам, насколько близка к идеалу вода, поступающая в вашу посудомойку.
Итак, в целом, по уровню жесткости вода в г. Москва подходит для посудомоечной машины. Однако в зимний период ситуация может измениться, поэтому не забывайте иногда заходить на сайт Мосводоканала для проверки. Удачи!

Какая вода в Москве — жесткая или мягкая? Жесткость воды — одна из основных ее проблем, указывающая на чрезмерное количество солей магния, кальция и железа. Существует несколько способов измерения жесткости воды. В соответствии с общепринятой системой СИ единицей измерения концентрации катионов магния и кальция в воде является моль на куб. Однако на практике гораздо чаще используются такие единицы, как миллиграмм на литр и градус жесткости.
Дорогие читатели! Наши статьи рассказывают о типовых способах решения юридических вопросов, но каждый случай носит уникальный характер.
Если вы хотите узнать, как решить именно Вашу проблему — обращайтесь в форму онлайн-консультанта справа или звоните по телефонам, представленным на сайте. Это быстро и бесплатно!
Например, в Санэпидемстанцию. СЭС проверит не только концентрацию солей жесткости, но и зафиксирует нитраты, пестициды, уровень содержания железа, сероводород, органические примеси и другие вещества, которые часто встречаются в грунтовых водах.
Пей, москвич, козленочком не станешь! RU, Москва, 27 февраля Автор: Александра Крылова Мы взяли воду из крана в разных округах столицы и отправили на анализ. Воду мы отвезли в лабораторию компании «Экостандарт».
Жёсткая и мягкая: какая вода вреднее для организма
Получить консультацию Грунтовые воды, проходя через слои известковых пород, вымывают соли кальция и магния и растворяют минеральные вещества, которые составляют основу вхождения. По вине высокой концентрации солей магния и кальция, жесткой воде присуще такое неприятное качество, как оседание налета на дне и стенках посуды, тонкая пленка на волосах, плохое мыление мыла, засорение водопровода и систем водонагрева.
При употреблении такой влаги для питья, жажда утоляется намного быстрее и на продолжительное время, чего не скажешь о мягкой воде. По итогам проведенных исследований, выяснилось, что в районах с жесткой водой смертность от заболеваний сердца несколько ниже, но медицина считает, что такая вода оказывает отрицательное действие на сердце, артерии и кости.
В этих органах при помощи жесткой воды остаются кальциевые отложения. Поэтому водоподготовка такой жидкости обязательно должна включать умягчение воды. Какие непрятные моменты может принести нам жесткость водопроводной воды?
Соли, находящиеся в воде, оседают на волосах липким налётом, появляется сухость, ломкость волос и перхоть головы; жёсткую воду нельзя применять в некоторых технологических процессах.
Например, на производстве по изготовлению пива или при покраске водорастворимыми красками; жёсткая вода, препятствует хорошему пенообразованию, что приводит к большему расходу моющих средств; при употреблении жесткой воды для стирки, очень сложно сделать качественное прополаскивание. Белые тона — приобретают сероватый оттенок, цветные ткани — тускнеют, провести отбеливание почти невозможно; нагревательные элементы электрочайников, посудомоечных и стиральных машин выходят из строя под воздействием образующегося известкового налёта; время приготовления некоторых продуктов в жёсткой воде значительно дольше.
Ионы кальция в соединении с белками дают нерастворимые соединения; употребив жёсткую воду можно испортить как цвет, так и вкус кофе и чая; в системах отопления, водопроводных трубах, использование жесткой воды приводит к образованию известняковых наростов, этим снижается энергоэффетивность и напор воды, преждевременно выходит из строя оборудование; такое же негативное влияние оказывает жесткая вода и на котельное оборудование.
Жесткая вода, может нанести вред не только человеку, но и растениям и аквариумным рыбкам. Каждая хозяйка знает, что для полива комнатных растений, замены воды в аквариуме, рекомендуют использовать только отстоявшуюся жидкость. Но никто особо не задумывался почему. А все по вине тех же солей, присутствующих в водопроодных системах.
Поэтому лучше использовать для очищения воды фильтры бытового назначения , очищающие и смягчающие воду. Природные воды и жесткая и мягкая, имеют возможность изменения свого состава несколько раз на год.
Влага испаряется, вода становится жестче, идут дожди или тает снег, вода становится мягче. Употреблять жесткую нужно в умягченном состоянии.
Каждый конкретный источник, из которого подается вода по водопроводу к потребителю, имеет свою жесткость воды, но он, неизменим при подготовительном процессе питьевой воды для систем центрального водоснабжения. Все сведения о жесткости водопроводной воды находятся непосредственно на водоканале и в санэпидстанции населенного пункта, потребляющего продукт центрального водогона. Для определения жесткости воды в домашних условиях изобрели специальные приборы, определяющие уровень наличия солей в воде.
Стандарт допустимой жесткости в центральном водоснабжении это 7 миллиграмм эквивалента на 1 литр. А для мошашней водоподготовки рекомендуют использовать фильтр умягчитель. С января года в России введен и уже работает новый стандарт жесткости воды.
Жесткость питьевой воды в Москве
Какая вода лучше — жесткая или мягкая 26 сентября Вода — это стихия, без которой не может прожить ни одно живое существо, она может как спасти, так и уничтожить. В быту очень важно, какую жидкость вы используете — жесткую или мягкую. Тут поневоле задумаешься, в чем их разница? Стоит ли вообще пить неочищенную жидкость? Стоит ли пользоваться водопроводной влагой даже для мытья посуды, умывания и стирки? Жесткость жидкости зависит от процентного содержания в ней солей кальция, магния и углекислого газа. Соотношение это бывает временным и постоянным.
Пей, москвич, козленочком не станешь!
Какая вода в Москве — жесткая или мягкая? Особенно вода, так как в день необходимо употреблять 2 литра. Вода, которая имеет большое количество примесей, негативно воздействует на организм человека, отсюда и появляются различные заболевания.
Дистиллированная вода является продуктом человеческой деятельности, и пить ее вместо обычной воды ни в коем случае нельзя — это приведет к вымыванию из организма жизненно важных солей, минералов и микроэлементов. Откуда берут воду для Москвы?
Как определить жесткость воды
Аммоний в питьевой воде появляется, в основном, в результате процесса обеззараживания с использованием аммиачной воды. Не относится к агентам, непосредственно влияющим на здоровье человека. Являются частью азотного цикла и показателем фекального загрязнения воды. Употребление воды с повышенным содержанием нитритов и нитратов приводит к нарушению функции крови. Опасность нитратов обусловлена их токсичным действием на организм. Содержание в сырой поверхностной воде обычно достаточно низкое, но грунтовые и подземные воды могут содержать высокие концентрации фторидов.
Качество воды в районах Москвы
Получить консультацию Грунтовые воды, проходя через слои известковых пород, вымывают соли кальция и магния и растворяют минеральные вещества, которые составляют основу вхождения. По вине высокой концентрации солей магния и кальция, жесткой воде присуще такое неприятное качество, как оседание налета на дне и стенках посуды, тонкая пленка на волосах, плохое мыление мыла, засорение водопровода и систем водонагрева. При употреблении такой влаги для питья, жажда утоляется намного быстрее и на продолжительное время, чего не скажешь о мягкой воде. По итогам проведенных исследований, выяснилось, что в районах с жесткой водой смертность от заболеваний сердца несколько ниже, но медицина считает, что такая вода оказывает отрицательное действие на сердце, артерии и кости.
Фильтруй не фильтруй. Специалисты рассказали правду о водопроводной воде

Итак, чистая h3O не течет ни из одного крана в мире — там всегда присутствуют растворенные соли, которые и определяют ее свойства, это зависит от наличия щелочноземельных металлов. Хотите пить чистую воду и получать от этого выгоды для своего организма? Водный состав с большим содержанием таких солей относится к жесткой, а с малым — к мягкой. Так какая лучше? Рассмотрим этот вопрос поподробнее. Отличие жесткой воды от мягкой Жёсткую h3O вредно пить в больших количествах, так как это приводит к отложению солей в суставах и в почках.
Контакты Какая вода в Москве: жёсткая или мягкая? Многих жителей столицы волнует вопрос: какая вода в Москве — жёстка или мягкая?
Поделив граммы на литры получаем: Кипячение устраняет только временную карбонатную жёсткость. Находит применение в быту. Реагентное умягчение. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Этот метод оправдан при относительно больших расходах воды, поскольку связан с решением ряда специфических проблем: фильтрации осадка, точной дозировки реагента. Метод основан на использовании ионообменной гранулированной загрузки чаще всего ионообменные смолы. Такая загрузка при контакте с водой поглощает катионы солей жёсткости кальций и магний, железо и марганец. Взамен, в зависимости от ионной формы, отдаёт ионы натрия или водорода.
Этот феномен объясняется, с одной стороны, сорбцией тканью кальциевых и магниевых солей жирных кислот, образующихся в процессе стирки на макроуровне. Жёсткая вода при умывании сушит кожу, в ней плохо образуется пена при использовании мыла. Использование жёсткой воды вызывает появление осадка накипи на стенках котлов, в трубах и т. В то же время, использование слишком мягкой воды может приводить к коррозии труб, так как, в этом случае отсутствует кислотно — щелочная буферность , которую обеспечивает гидрокарбонатная временная жёсткость. Жёсткость природных вод может варьироваться в довольно широких пределах и в течение года непостоянна. Увеличивается жёсткость из-за испарения воды, уменьшается в сезон дождей, а также в период таяния снега и льда.
Это неправильно. Конечно, они не имеют отношения к сказкам и мифам о целебности живой воды и губительности мертвой. Просто существуют теории, пока не получившие официального признания, но и не опровергнутые, что вода со щелочной реакцией имеет некоторые полезные свойства, ее и называют живой. Кислотную воду, соответственно, называют мертвой. С мягкостью или жесткостью воды это связано мало. Почему вещи становятся жесткими после стирки в жесткой воде? Потому, что соли забивают поры нитей, делая их менее эластичными и грубыми. Кроме того, жесткая вода придает вещам неприятный серый или желтоватый оттенок, портит их цвет.

Поэтому перед человеком встает задача по определению уровня жесткости воды, которую нужно быстро решать в условиях быта. Для этого требуется знать, что же представляет собой жесткая вода, в каких единицах она измеряется, какие способы можно использовать, чтобы быстро определить степень жесткость воды. Жесткость воды: что это такое?